
脓毒症是机体对感染的反应失调导致危及生命的器官功能障碍。脓毒症是危重患者死亡的最常见原因,据估计2020年中国脓毒症导致近100万人死亡,脓毒症相关死亡率从2006年的130.2/10万下降至2020年的76.6/10万,脓毒症的诊断通常依赖于临床表现和相关评分系统,如《脓毒症和
长期过量饮酒是ALD的主要致病因素,有研究表明有害饮酒(男性饮酒3杯/天或21杯/周,女性2杯/天或14杯/周)是ALD的危险因素。ALD的疾病谱包括脂肪变性、酒精性肝炎(AH)、进行性
ALD致脓毒症易感性增加的具体机制包括免疫功能障碍、肠道屏障功能破坏、
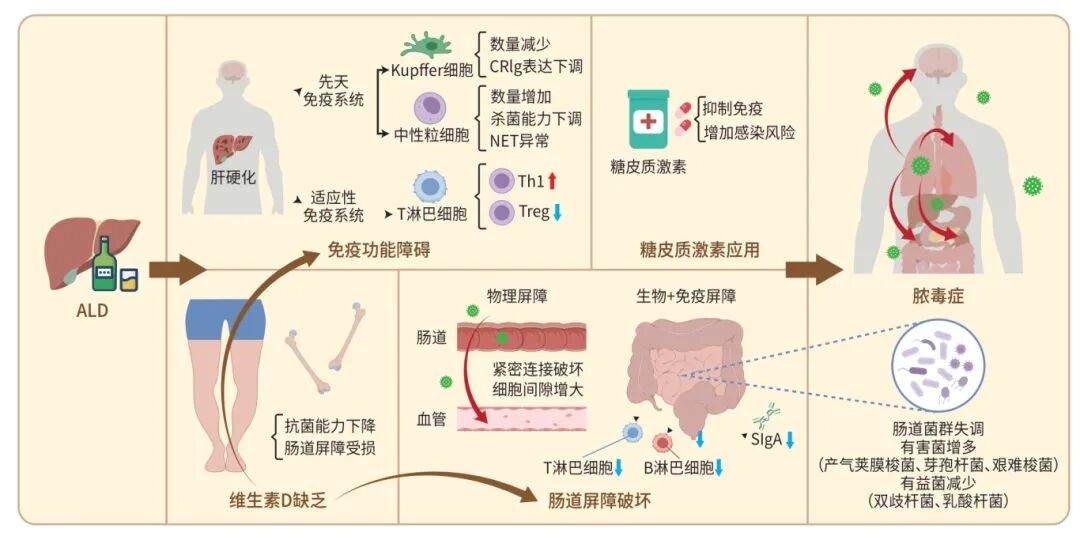
注: CRIg,免疫球蛋白超家族补体受体;NET,中性粒细胞胞外陷阱;Th1,辅助性T淋巴细胞1型;Treg,调节性T淋巴细胞;SIgA,分泌型免疫球蛋白A。
图1 ALD增加脓毒症易感性的机制

1免疫系统障碍
ALD患者的病程常伴随着肝硬化,导致肝脏调控机体内环境稳态的功能受损,从而出现肝硬化相关的免疫功能障碍(CAID)。CAID的显著特征是获得性免疫缺陷和全身炎症的动态共存,这是肝硬化对脓毒症易感性增加的病理生理学特征。CAID影响先天免疫系统及适应性免疫系统,几乎所有细胞类型都出现紊乱。先天免疫系统的细胞包括中性粒细胞、单核细胞、组织驻留和募集的巨噬细胞、树突状细胞和自然杀伤细胞。适应性免疫系统由不同的
Kupffer细胞是肝脏的常驻巨噬细胞,主要通过吞噬作用清除外来物质和死亡细胞。Kupffer细胞通常是最先接触由酒精引发的肠道来源微生物免疫原性刺激的细胞之一,这些刺激包括脂多糖(LPS)和肽聚糖。Kupffer细胞的激活是ALD发病机制中的关键环节,饮酒期间细菌LPS的肠道移位增加是诱导Kupffer细胞激活的关键,酒精摄入引起的肠道通透性增加和肝细胞损伤会导致病原体相关分子模式或损伤相关分子模式的释放,这些分子通过Toll样受体(TLR)通路激活炎症反应,从而加重AH。LPS与Kupffer细胞表面的TLR4结合后,通过激活MyD88依赖性和TRIF依赖性信号通路,触发下游的MAPK(丝裂原活化蛋白激酶)和NF-κB(核因子κB)信号级联反应。这一过程导致Kupffer细胞释放促炎细胞因子TNF-α、IL-1β、IL-12、IL-18和IL-23,同时分泌趋化因子C-X-C基序趋化因子配体1和单核细胞趋化蛋白-1,进而招募中性粒细胞和单核细胞,加剧肝脏炎症反应。肽聚糖通过与TLR2受体或NOD样受体结合,通过激活MyD88依赖性或RIP2(受体相互作用蛋白激酶2)依赖性信号通路,导致免疫细胞释放TNF-α、IL-1β、IL-6、IL-12及IL-10,加剧炎症反应。CRIg主要表达于肝脏Kupffer细胞和其他组织驻留的巨噬细胞。Kupffer细胞通过CRIg识别和吞噬补体分解产物C3b和iC3b,清除血液中的病原体,防止细菌性脓毒症发生。也有研究表明,CRIg可作为巨噬细胞模式识别受体,直接结合并捕获血源性革兰阳性菌。Duan等研究发现,ALD患者肝脏CRIg的表达降低,CRIg缺陷小鼠对肠道移位的革兰阳性菌清除能力显著降低,且酒精喂养后
肝脏可以有效监测并清除血液中来自肠道的分子和病原体,从而维持体内免疫稳态。肝硬化通常伴随肝脏的结构损害,如肝窦纤维化和毛细血管化、伴随门体分流形成的间隔纤维化以及Kupffer细胞功能障碍,这些特征在酒精性肝硬化中更加明显。Peiseler等发现与对照组小鼠相比,肝纤维化小鼠在感染
ALD患者Kupffer细胞数量减少、CRIg表达下调及肝纤维化微环境共同导致Kupffer细胞吞噬功能缺陷,使其无法有效清除肠道来源的细菌颗粒,导致脓毒症感染风险增加。
AH通常伴随着循环系统和肝脏的中性粒细胞计数增加。中性粒细胞是数量最多的先天免疫细胞,占人类所有循环白细胞的40%~75%,配有储存在专门颗粒中的抗菌剂,可通过吞噬作用、脱颗粒和释放中性粒细胞胞外陷阱(NET)来释放这些抗菌剂,是抵御细菌感染的第一道防线,在先天免疫系统中发挥重要作用。中性粒细胞功能障碍显著增加了ALD患者的感染风险,脓毒症相关器官衰竭仍然是ALD患者死亡的主要原因。AH 中观察到循环中性粒细胞和肝中性粒细胞增加,但中性粒细胞静息氧化爆发能力及吞噬功能受损,导致细菌清除能力下降,感染的易感性增加。Mookerjee等对63例肝硬化合并AH患者的中性粒细胞功能的研究发现,中性粒细胞功能障碍表现为静息氧化爆发≥55%且吞噬能力<42%,与感染、脏器衰竭及死亡风险显著相关,这种功能障碍的原因可能与循环LPS的增加有关,并且可能通过去除LPS或使用TLR4抑制剂恢复中性粒细胞的功能。
NET在感染过程中可能发挥双重作用:一方面通过直接捕获和杀死细菌、真菌和病毒等微生物,起到免疫防御作用;另一方面过度释放NET可能加重炎症反应。Bukong等对健康志愿者的中性粒细胞进行酒精处理后发现,NET形成增加,但在PMA(佛波醇12-肉豆蔻酸酯13-乙酸酯)进一步刺激下,NET生成能力却下降,表明酗酒诱导了中性粒细胞功能的耗竭。同时在酗酒小鼠模型中,肝脏中性粒细胞迁移显著减少,NET形成的关键组分(如瓜氨酸化组蛋白H3和中性粒细胞弹性蛋白酶)的表达也下降;并且酗酒小鼠的肝脏中性粒细胞及NET的清除显著受损,导致肝脏内促炎因子水平升高以及肝细胞凋亡加剧,从而加剧肝损伤和脓毒症严重程度。另一项研究发现在酒精相关性肝炎患者血液中NET显著增加,中性粒细胞表型改变,高密度中性粒细胞被激活而低密度中性粒细胞存在缺陷;低密度中性粒细胞表现为功能耗竭表型,在静息和LPS刺激下表现出活性氧生成减少,吞噬能力下降,且被巨噬细胞清除减少。
中性粒细胞在ALD中表现为功能障碍,数量增加但微生物清除能力降低,同时伴随NET异常生成,导致机体抗感染能力下降、脓毒症易感性增加,监测和改善ALD患者的中性粒细胞功能可能成为治疗ALD患者脓毒症的方向。
适应性免疫细胞在机体形成免疫记忆并对抗原和炎症信号产生持久免疫反应中发挥重要作用。T淋巴细胞是适应性免疫细胞的重要组成部分,同时又作为肝脏募集的循环免疫细胞,在ALD的炎症反应中发挥着关键作用。成熟T淋巴细胞分为CD4+和CD8+亚型,过量的酒精摄入会导致T淋巴细胞免疫表型发生变化,从而削弱机体对损伤的防御能力,增加感染风险。McTernan等的研究表明酒精可通过影响 CD4+ T淋巴细胞的免疫代谢,促使CD4+ T淋巴细胞向促炎表型(如Th1)分化,并抑制Treg分化,从而加剧全身性炎症反应。Zuluaga等研究发现酒精性肝硬化患者CD4+ T淋巴细胞的分化能力丧失,饮酒会促使细胞向Th1/Th2表型分化,Th17减少。这种T淋巴细胞分化失调可能降低抗原识别能力,从而增加细菌感染风险。

2肠道屏障功能障碍
肠道是人体表面积最大的屏障器官,能保护机体免受潜在有毒代谢物、细菌及其抗原的侵害。肠道屏障是一个复杂的结构,主要由肠道微生物群、不动水层、糖萼、黏膜层以及由紧密连接蛋白连接的上皮细胞组成。酒精破坏肠道上皮屏障,包括物理屏障、免疫屏障和生物屏障,增加肠道通透性,从而促进细菌和细菌产物进入全身循环。肠道屏障破坏被称为“肠漏”或肠壁漏综合征,其特征是细菌代谢物和内毒素释放到循环中。肠道屏障功能的完整性对于维持机体健康非常重要,其破坏会造成局部或全身炎症,从而造成组织器官损伤。Tulkens等的研究表明,肠道屏障功能障碍患者的血浆中LPS阳性细菌细胞外囊泡水平显著高于健康对照组,并能够诱导免疫激活,表现为促炎细胞因子分泌增加。
紧密连接是由一组复杂的蛋白质网络构成,包括occludin、claudin和连接黏附分子,这些蛋白质通过ZO-1等蛋白与肌动蛋白细胞骨架相互作用。紧密连接对屏障功能非常重要,肠上皮细胞紧密连接破坏是酒精相关脓毒症、全身炎症和多器官损伤的主要诱因。Meena等的研究发现,酒精及其有毒代谢产物通过刺激TRPV6通道介导的钙离子吸收,增加细胞内钙离子浓度,从而破坏肠上皮细胞间紧密连接,导致肠上皮屏障功能障碍;使用TRPV6基因敲除小鼠或TRPV6特异性抑制剂可以减轻酒精诱导的肠屏障功能障碍及肝损伤。Rungratanawanich等对ALDH2基因敲除小鼠和野生型小鼠研究发现,低剂量(3.5 g/kg)酒精喂养1 h可以引起ALDH2基因敲除小鼠肠道炎症和肠上皮细胞凋亡以及血清内毒素水平升高;酒精暴露使小鼠肠道紧密连接和黏附连接蛋白(如ZO-1、Occludin等)显著降低,同时肠道菌群中有益菌减少、致病菌增加,而野生型小鼠变化较小。
肠道免疫屏障主要由SIgA和肠道相关淋巴组织组成。肠道黏膜免疫系统通过协调先天性和适应性免疫反应来清除潜在的致病微生物。肠道T淋巴细胞和B淋巴细胞在ALD肠道屏障功能障碍中发挥重要作用。SIgA由肠道固有层中的
肠道是人体最大的微生物储存库,包括各种微生物如细菌、古细菌、真菌和病毒,它们参与消化、物质代谢和宿主免疫。肠道微生物群主要由两大类优势菌群构成,分别是作为革兰阳性菌代表的厚壁菌门,以及属于革兰阴性菌的拟杆菌门。肠道、肝脏和免疫系统与肠道微生物有着共生关系。饮酒会造成肠道微生物群组成及功能改变导致
酒精通过破坏肠道上皮屏障功能,使肠道通透性增高,肠源性微生物和细菌内毒素进入门静脉及体循环,导致全身炎症及脓毒症易感性增加。因此,保护ALD患者肠道屏障功能可能使患者感染风险下降,改善预后。

3维生素D缺乏(VDD)
维生素D除调节骨代谢外,还具有抗菌活性与免疫调节特性,同时也是维持紧密连接及黏附连接完整性的辅助因子。酗酒人群中普遍存在VDD,多项研究表明,VDD在慢性肝病,尤其是在酒精相关肝病中极为普遍。VDD可以增加脓毒症的发生和死亡风险。Parekh等的研究纳入61例轻度脓毒症和重症脓毒症患者及20例健康对照者,结果发现重症脓毒症患者的25-羟维生素D3浓度显著低于轻度脓毒症患者和健康对照组;同时动物实验表明,VDD小鼠模型细菌载量显著增加,并伴随抗菌肽表达降低和巨噬细胞吞噬功能缺陷。Wang等发现VDD可以改变饮酒小鼠肠道菌群组成,导致肠道紧密连接蛋白Occludin和E-cadherin的蛋白表达下调,同时促进肝脏和结肠组织中炎性细胞因子的表达上调。Shibamoto等开展的研究对78例ALD相关肝硬化患者进行了分析,显示ALD相关肝硬化患者血清25-羟基维生素D水平显著低于健康对照组,且内毒素活性显著升高;同时小鼠实验中维生素D缺乏使小鼠肠道的紧密连接蛋白如ZO-1、occludin、claudin-2等表达显著下调,肠道通透性增加,同时肝脏LPS水平升高,表明了VDD与ALD相关肝硬化患者的内毒素血症相关。
VDD导致ALD肠道菌群破坏、肠道通透性增加以及炎症反应激活,可能使脓毒症感染的机会增加。然而这些改变在ALD患者中同样存在,尚未明确维生素D在ALD相关脓毒症进程中如何与其他因素相互作用,仍有待深入探索。

4糖皮质激素治疗
糖皮质激素是治疗sAH的主要方法之一,能提高短期生存率,但对于其是否增加感染风险仍存在争议。糖皮质激素治疗可能引发剂量依赖性不良反应,尤其在脓毒症感染风险上,糖皮质激素通过抑制中性粒细胞趋化功能、下调促炎细胞因子(如TNF-α、IL-1β)表达,并阻碍免疫细胞向感染灶的募集,削弱了机体的免疫防御机制。该免疫抑制作用可进一步恶化sAH患者固有的免疫麻痹状态,糖皮质激素的使用可能使患者更易发生感染事件。Vergis等通过对1 092例sAH患者的研究发现,泼尼松治疗会增加sAH患者严重感染和治疗后感染风险,且感染与泼尼松治疗患者的90天病死率独立相关;同时还发现治疗前循环细菌DNA水平>18.5 pg/mL可预测泼尼松治疗患者的7天内感染风险。Thursz等对1 103例sAH患者进行多中心双盲随机试验发现,泼尼松治疗增加了sAH患者感染风险,但不会增加感染相关病死率。
糖皮质激素可以改善sAH的短期预后,但其带来的感染风险不能忽视,在sAH患者治疗中需要权衡糖皮质激素的使用时机、剂量和治疗时长,并监控治疗期间的感染风险,同时也需要研究糖皮质激素的替代疗法。

5结语与展望
综上,脓毒症是ALD患者最常见的并发症和死亡原因之一,ALD可通过多种途径增加脓毒症易感性,如免疫功能障碍、肠道屏障功能破坏、VDD及糖皮质激素诱导的获得性免疫抑制等。ALD通过削弱先天性及适应性免疫细胞的功能使其对病原体清除能力下降,并且损害肠道屏障功能导致肠道微生物群改变、肠道通透性增高,使得肠源性微生物和细菌内毒素进入门静脉及体循环,同时ALD病程中往往存在营养不良如VDD、糖皮质激素治疗导致的免疫抑制状态,这些因素共同导致了ALD患者的脓毒症高感染风险。虽然有大量研究已揭示ALD相关脓毒症的部分关键机制,但对免疫平衡变化的调控机制、宿主-微生物协同作用、遗传易感性差异等关键科学问题仍需通过多中心队列研究结合单细胞测序/代谢组学技术深入解析,未来方向应聚焦信号传导路径的作用机制、循环miRNA生物标志物筛选及菌群定向移植等精准干预方案的构建,以降低ALD患者脓毒症发生率,提高生存率。

https://www.lcgdbzz.org/cn/article/doi/10.12449/JCH250829

刘航, 郭焱. 酒精性肝病增加脓毒症易感性机制的研究进展[J]. 临床肝胆病杂志, 2025, 41(8): 1662-1667
来源:临床肝胆病杂志
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
