根据是否存在MM前驱病史,PCL可分为pPCL和继发性PCL(secondary PCL,sPCL)两类。2021年国际骨髓瘤工作组(IMWG)更新了pPCL的诊断标准,将外周血循环浆细胞(circulating plasma cell,CPC)阈值从20%下调至5%。更新后的pPCL定义为在满足MM诊断标准的基础上,外周血CPC≥5%的恶性浆细胞疾病,约占新诊断MM(newly diagnosed MM, NDMM)患者的6% 。sPCL则发生于既往确诊的MM患者中,多见于多线治疗后的复发难治性MM(relapsed/refractory MM,RRMM)患者,占RRMM病例的1%,其中位生存期仅1~4个月 。需要说明的是,目前sPCL的CPC诊断阈值尚未完全统一,但越来越多的研究采用5%作为临界值 。
pPCL的中位发病年龄为52~65岁,较MM患者发病年龄低约10岁。在其M蛋白类型中,轻链型和不分泌型更为常见。pPCL起病急,肿瘤负荷高,症状显著,常伴严重
pPCL细胞在形态学、免疫表型和遗传学特征上与典型MM细胞有所不同 。形态学方面,pPCL细胞常表现为淋巴细胞样或浆母细胞样形态。免疫表型方面,pPCL细胞中CD56表达显著下调,而CD20、CD44、CD45和CD19的表达水平升高,同时CD11a、CD27、CD28、CD81、CD71、CD9、HLA-DR和CD117的表达降低。上述黏附分子表达失衡导致浆细胞与骨髓微环境的相互作用减弱,因此肿瘤细胞更易进入外周血循环。从细胞遗传学特征来看,pPCL亚二倍体常见,同时t(11;14)、t(14;16)等
PCL的诊断应建立在MM的基础上,因此所有新诊断患者都应进行MM相关检查。 表1 列出了诊断PCL必备的检查项目 。
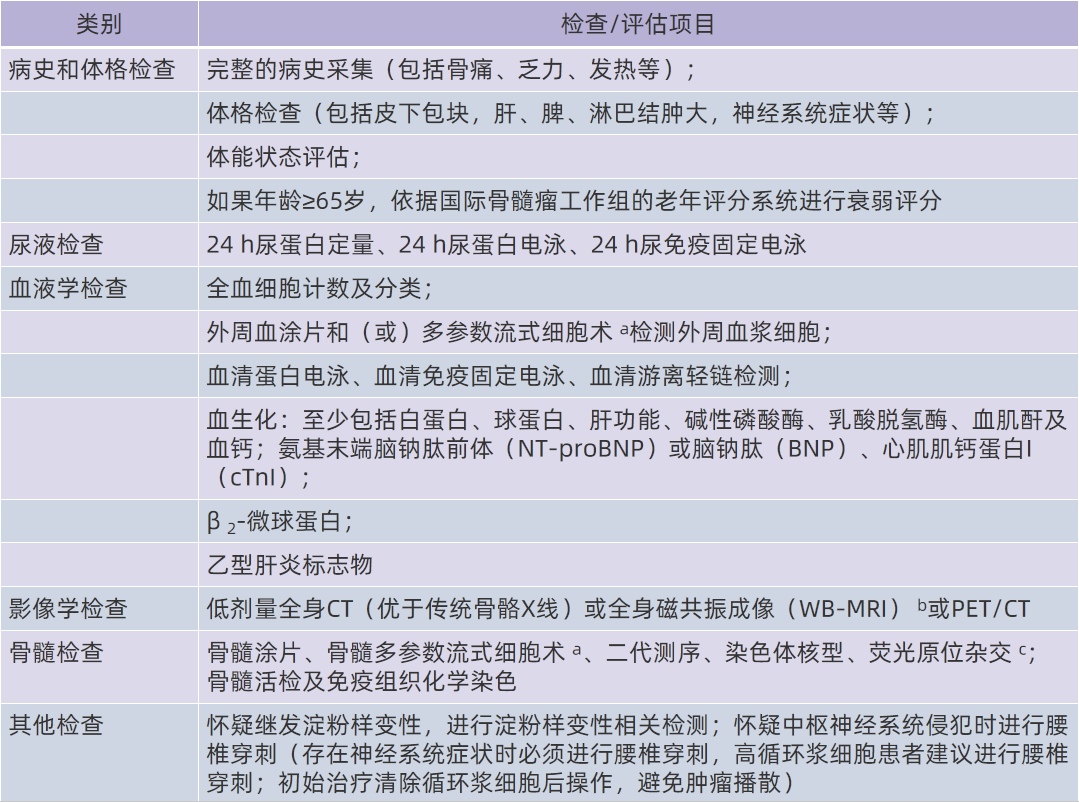
表1 诊断浆细胞白血病(PCL)时必需的检查类别及项目
注: a怀疑PCL的患者应进行外周血多参数流式细胞术检测,以CD45 -/dimCD38 +细胞设门,同时应包括CD138、CD56、CD19、CD27、CD20、CD81、CD117、HLA-DR及胞质κ和λ、BCMA、GPRC5D; bWB-MRI尤其是弥散加权MRI对于识别髓外病灶具有较高的灵敏性; c荧光原位杂交检测前建议用CD138磁珠分选肿瘤细胞,检测位点建议包括:IgH重排、17p缺失、13q14缺失、1q21增加/扩增、1p32缺失、Myc易位,若IgH重排阳性,则进一步检测t(4;14)、t(11;14)、t(14;16)、t(14;20)
专家共识:①PCL的诊断应在MM基础上进行,所有新诊断患者均需完成MM相关检查。②怀疑PCL患者应进行外周
所有pPCL均应视为超高危的浆细胞肿瘤。目前pPCL尚未建立统一的标准化分期及危险度分层系统,建议参考MM的风险评估框架。有研究提出简化评分模型,纳入三项危险因素:年龄>60岁、血小板计数<100×109/L以及外周血CPC>20×109/L。根据该模型,无危险因素患者的中位OS期为46个月,含1项危险因素者OS期降至27个月,而具有2项及以上危险因素者OS期仅12个月 。研究显示,伴有高危细胞遗传学异常的pPCL患者预后更差,但t(11;14)阳性PCL患者的预后优于t(11;14)阴性者。
专家共识:①pPCL目前缺乏统一的预后分期系统,临床评估需综合以下因素:患者年龄、CPC水平、血小板计数及细胞遗传学异常。②值得注意的是,携带t(11;14)染色体易位的pPCL患者通常预后较好。
由于pPCL相对少见,目前尚缺乏大规模前瞻性临床试验,因此其标准治疗尚未确定。专家委员会认为,pPCL的总体治疗策略包括以下三点:①采用不同作用机制的多种药物联合治疗,并持续治疗;②以根除所有肿瘤克隆为目标,尽可能实现并维持骨髓内外微小残留病(minimal residual disease,MRD)阴性状态;③鉴于pPCL当前疗效有限,建议优先入组符合条件的临床试验。
(1)移植前的诱导治疗:在pPCL中,诱导治疗不仅用于快速控制高肿瘤负荷,更应力求实现深度缓解,甚至达到MRD阴性,从而为后续的移植和长期疾病控制奠定基础。鉴于pPCL临床进展迅速,且对标准治疗方案反应不佳,建议尽早采用强化诱导方案,推荐以CD38单克隆抗体、蛋白酶体抑制剂、免疫调节剂及
(2)造血干细胞移植:作为整体治疗的基石,auto-HSCT可增加pPCL患者治疗深度并延长生存期 。串联移植(tandem transplantation)指在第一次auto-HSCT后的6个月内进行计划中的第2次auto-HSCT。既往研究表明,pPCL患者可能从串联移植中获益。建议患者在首次动员后尽量采集满足两次auto-HSCT所需的造血干细胞数量,建议第一次移植后6个月内进行串联移植。两次移植采用的预处理方案通常为大剂量
(3)巩固治疗:串联自体移植后,若仍未达到CR和(或)MRD阴性,建议采用原诱导方案继续巩固治疗2个疗程;若2个疗程后仍未达到CR和(或)MRD阴性,可延长至4个疗程。对于已达到CR和(或)MRD阴性的患者,可考虑不进行巩固治疗。若患者未接受串联移植,则建议采用原诱导方案继续巩固治疗2~4个疗程 。
(4)维持治疗:推荐采用免疫调节剂、蛋白酶体抑制剂和(或)CD38单克隆抗体为基础的两药或三药方案进行维持治疗,持续治疗直至疾病进展或不能耐受。
专家共识:适合移植的pPCL治疗:①符合条件的患者优先纳入临床试验,尤其是包含CAR-T细胞治疗及双特异性抗体的临床试验。②在pPCL移植前,推荐采用含CD38单克隆抗体、蛋白酶体抑制剂、免疫调节剂及地塞米松的四药联合方案作为诱导治疗。具体方案包括:CD38单克隆抗体+VRd/KRd。对于体能状态良好、年轻且肿瘤负荷较高者,可使用CD38单克隆抗体+VRD/KRD-PACE或CD38单克隆抗体+DECP。③造血干细胞移植:<50岁,有合适供者:串联auto-HSCT或清髓性allo-HSCT或auto-HSCT序贯减低强度非清髓性allo-HSCT。<50岁,无合适供者:串联auto-HSCT。>50岁,有合适供者:串联auto-HSCT或auto-HSCT序贯减低强度非清髓性allo-HSCT。>50岁,无合适供者:串联auto-HSCT。④巩固治疗:若患者未接受串联移植或串联移植后未达到CR或MRD阴性,建议沿用原诱导方案巩固治疗2~4个疗程。⑤维持治疗:推荐应用含免疫调节剂、蛋白酶体抑制剂和(或)CD38单克隆抗体的两药或三药方案进行维持治疗,建议持续治疗直至疾病进展或不能耐受。⑥pPCL具有较高的中枢神经系统侵犯风险。如患者出现神经系统症状,应进行诊断性腰椎穿刺。为了避免肿瘤细胞播散至中枢神经系统,腰椎穿刺最好在初始治疗后待浆细胞减少或消失后再进行。
对于不适合移植的pPCL患者,首选临床试验。有临床试验正在探索CAR-T细胞治疗初诊不适合移植的pPCL患者。若无临床试验可选,需根据IMWG虚弱程度分级(GA评分)进行体能状态评估,并制定个体化治疗方案。对于体能状态良好的患者,优先推荐以CD38单克隆抗体为基础的四药联合方案(联合蛋白酶体抑制剂、免疫调节剂及地塞米松);针对虚弱患者,则采用CD38单克隆抗体联合蛋白酶体抑制剂或免疫调节剂的三药方案(含地塞米松)。建议持续治疗至疾病进展或出现不可耐受的不良反应。
专家共识:①优先考虑入组临床试验,尤其是包含CAR-T细胞治疗和双特异性抗体的临床试验。②推荐所有不适合移植的pPCL患者先行老年体能状态评估;对于体能状态良好的患者,推荐采用CD38单克隆抗体联合蛋白酶体抑制剂、免疫调节剂及地塞米松的四药联合方案持续治疗;对于体能状态较差或合并基础疾病的体弱患者,建议采用以CD38单克隆抗体为基础的三药联合方案持续治疗。
复发/难治pPCL患者预后极差,当前尚无统一标准治疗方案。治疗策略应综合既往用药、缓解深度、复发时间、年龄及体能状态等因素。根据年龄和体能状态,推荐联合既往未应用过的药物(如新一代蛋白酶体抑制剂、免疫调节剂、CD38单克隆抗体等)治疗。对挽救性治疗有反应且符合移植标准的患者,建议进行allo-HSCT;不适合进行移植的患者建议继续接受治疗,直至疾病出现进展或患者无法耐受治疗。对于携带t(11;14)易位的患者,可以考虑采用BCL-2抑制剂进行单药或联合治疗。此外,多项小队列回顾性研究证实CAR-T细胞治疗对复发难治pPCL患者有良好的疗效。双特异性抗体作为即用型药物,在临床上可能有潜力控制pPCL快速进展。
专家共识:①推荐所有复发/难治pPCL患者优先考虑入组临床试验,尤其是免疫治疗的临床试验;②推荐复发/难治pPCL患者选择新一代药物或不同作用机制药物的联合方案。
sPCL是MM演变至终末期的临床表现,常在既往多线治疗后发生,呈现肿瘤克隆高度不稳定、快速进展和耐药等特征,预后极差。目前尚无公认的标准治疗方案,可参考pPCL的方案。多项小队列研究报道,CAR-T细胞治疗对于sPCL患者有一定的疗效,整体有效率近70% 。双特异性抗体对于治疗sPCL患者也具有一定的潜力,但疗效常难以持续 。
专家共识:①推荐sPCL患者优先考虑入组临床试验,尤其是免疫治疗的临床试验;②推荐sPCL患者选择未应用过的新一代药物或不同作用机制药物的联合方案。
目前,PCL建议参照IMWG关于MM的疗效标准,同时结合外周血CPC检测判断疗效。然而,鉴于PCL具有白血病特性,轻链型和无分泌型多见,且常合并髓外病变,传统疗效评估标准无法全面反映PCL患者的治疗反应。因此,建议联合应用下一代流式细胞术(next-generation flow,NGF)或下一代测序技术(next-generation sequencing,NGS)动态监测PCL患者骨髓MRD。此外,针对PCL中CPC的独特生物学特征及临床意义,建议通过NGF动态监测外周残留病(peripheral residual disease,PRD) 。
专家共识:①PCL疗效评估参照IMWG的MM标准,同时结合外周血CPC检测;②推荐PCL患者动态监测骨髓和外周血肿瘤细胞。
PCL是一种预后极差的高度侵袭性浆细胞疾病,具有独特的生物学特征,包括基因组不稳定性、高增殖性及髓外病变发生率高等。2021年IMWG更新了诊断标准,将外周血中CPC比例≥5%作为pPCL的诊断阈值,显著扩大了患者范围 。当前,新型治疗手段尤其是蛋白酶体抑制剂、免疫调节剂和CD38单克隆抗体联合auto-HSCT的应用已显著改善了PCL患者的预后。未来的治疗策略将突破传统化疗和靶向治疗框架,更聚焦于免疫疗法。CAR-T细胞疗法正逐渐成为PCL的一线治疗,为PCL患者提供了新的治疗选择 。随着诊断标准的更新、疾病生物学机制的深入研究以及治疗策略的持续优化,PCL患者有望获得更长的生存期与更好的生活质量。
参考来源:
中国临床肿瘤学会(CSCO)骨髓瘤专家委员会,中国抗癌协会(CACA)血液肿瘤专业委员会骨髓瘤与浆细胞疾病学组,中华医学会血液学分会浆细胞疾病学组. 浆细胞白血病诊断与治疗中国专家共识(2025年版)[J]. 中华血液学杂志,2025,46(08):691-696.DOI:10.3760/cma.j.cn121090-20250618-00283.如遇版权问题请联系删除。
声明:本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)