作者(翻译):黄浚峰 毛晓筱 宋新宇 陈迪非 李时悦
第一作者单位:广州医科大学附属第一医院呼吸与危重症医学科 广州呼吸健康研究院 国家呼吸医学中心
引用本文:黄浚峰, 毛晓筱, 宋新宇, 等. 欧洲呼吸学会肺泡蛋白沉积症诊疗方案[J]. 中华结核和呼吸杂志, 2025, 48(10): 919-927. DOI: 10.3760/cma.j.cn112147-20250506-00248.
摘要
肺泡蛋白沉积症(pulmonary alveolar proteinosis,PAP)是一种罕见综合征,由多种不同病因引起,其特征是肺部蛋白样物质异常积聚,导致进行性呼吸困难、低氧血症、呼吸衰竭风险增高以及早亡。诊断策略可包括胸部CT、支气管肺泡灌洗(bronchoalveolar lavage,BAL)、抗粒细胞-巨噬细胞集落刺激因子(granulocyte macrophage colony stimulating factor,GM-CSF)抗体检测、基因检测,必要时可行肺活检。治疗方案主要聚焦于清除肺部蛋白样物质,包括全肺灌洗(whole lung lavage,WLL)、GM-CSF补充治疗、利妥昔单抗、血浆置换及肺移植。本指南旨在为管理PAP患者的临床医师提供诊断和治疗指导。欧洲呼吸学会(European respiratory society,ERS)组建的工作组委员会由具备PAP经验的临床医师、方法学家及患者代表组成。该委员会依据《ERS临床实践指南手册》及GRADE(推荐分级的评估、制定与评价)方法制定本指南推荐意见。具体工作包括系统文献综述,并应用GRADE方法评估证据质量及推荐强度。委员会围绕5个PICO(患者、干预、对照、结局)问题及2个描述性问题(narrative questions,NQ)制订了具体的循证推荐意见。工作组委员会针对上述5个PICO问题制订了推荐意见,内容涵盖:采用WLL、GM-CSF补充治疗、利妥昔单抗、血浆置换及肺移植治疗PAP。此外,委员会还基于描述性问题,就GM-CSF抗体检测、诊断性BAL及活检的应用提出了推荐意见。除具体推荐外,委员会还提供了关于诊断性检查及治疗措施优先级/层次结构的信息。PAP的诊断依据胸部CT及BAL细胞学或肺组织学检查结果;而明确导致PAP的具体病因则需进行GM-CSF抗体检测或基因分析。目前有包括WLL和GM-CSF补充治疗在内的多种疗法可用于治疗PAP,但其支持性证据仍有限。
一、范围与目标
ERS指南为PAP患者的治疗提供了循证医学建议。由于PAP是由临床表型和致病机制完全不同的多种疾病引起的,我们重点围绕其关键诊断和治疗问题展开讨论。本指南的目标读者包括所有参与儿童/青少年及成人PAP诊疗的相关人员,涵盖呼吸内科专家、儿科医师、放射科医师、病理科医师,以及监管部门、制药企业和政策制定者等。本指南并非旨在替代合理的临床判断,使用时需结合具体临床情境进行解读或调整,尤其需要考虑诊断工具(如GM-CSF抗体检测)和治疗方案(如GM-CSF增补疗法)的可及性等因素。此外,这些建议应根据患者的看法、价值观和偏好、可用的专业知识以及临床问题的性质和严重程度进行综合考虑。
二、简介
三、方法
ERS肺泡蛋白沉积临床实践指南由ERS工作组(TF)根据ERS临床实践指南[5]和GRADE[6]方法提出的方法制定。工作组由 C.McCarthy(爱尔兰)、F.Bonella(德国)和 E. Bendstrup(丹麦)共同主持。工作组包括 17名呼吸医学专家、2名儿科医生、1名放射科医生、1名病理学家、2名指南方法学家(同时也是呼吸医学专家)以及 2名PAP患者代表(详见原文在线附录)。2名患者代表是工作组的正式成员,参与了所有推荐意见的制定。
本指南探讨了7个与PAP诊断和管理相关的临床问题。根据ERS流程[5],使用PICO格式提出了5个问题,以及2个描述性问题。针对每个问题,根据GRADE方法,选择与临床实践重要性相关的结果。只有被大多数小组成员评为关键或重要的结果才被纳入推荐意见的制订(详见原文在线附录)。PICO问题基于正式的系统综述、荟萃分析和现有证据的评估,而描述性问题则基于系统的文献检索(具体文献检索与系统文献综述的方法见原文在线附录)。
基于比较研究的PICO问题生成了GRADE证据概况,所有PICO问题生成了证据到决策(EtD)框架,而描述性问题仅生成了EtD框架(见原文补充附录)。对于PICO问题,使用GRADE方法对支撑各结局指标的证据体进行确定性评估,评估结果分为极低、低、中或高4个等级。证据确定性的评判需综合评估纳入研究的偏倚风险、不一致性、间接性、不精确性以及发表偏倚。对于描述性问题,根据更新的ERS指南,采用描述性综述方法。小组使用EtD框架通过共识和(或)投票制定推荐意见及其强度。推荐意见分为强推荐或有条件推荐。根据GRADE术语[6],强推荐使用“我们推荐”,而有条件推荐使用“我们建议”。
当小组确定干预的获益大于风险时,对该干预做出强推荐;当证据显示相反情况时,对该干预做出强反对推荐。强推荐表明大多数患者和医疗提供者会选择推荐或不推荐该干预。当小组不确定干预对大多数患者的获益大于风险时,对该干预做出有条件推荐;当证据显示相反情况时,对该干预做出有条件反对推荐。有条件推荐表明不同患者和医疗提供者可能对干预做出不同选择。除推荐意见外,还对每个PICO问题提出了具体考虑。这些考虑反映了工作组成员的当前实践并描述了他们的临床经验。每个PICO问题均提供了支持这些评论的证据。所有推荐意见、评论和算法均经过全体小组成员的审查和批准。
GRADE和EtD框架用于汇总相关证据和考虑因素,包括干预措施的潜在获益和危害、现有证据的确定性、患者的价值观和偏好、所需资源以及公平性、可接受性、可行性和成本效益等考虑因素。这些框架在共识会议前与小组成员共享以供审阅,证据也在会议期间进行了展示和讨论。一旦所有小组成员,包括患者代表,确认信息已得到充分解释、讨论和报告,便通过公开投票制定推荐意见。多数票足以发布有条件推荐,而发布强推荐则需要至少70%的参与者同意。
四、疾病活动性、严重程度和进展的定义
(一)总体考虑
为提供规范化的管理建议,工作组基于现有文献及PAP诊疗中心的经验,为读者整理了相关的临床定义。
PAP的特征是肺泡中表面活性物质的进行性积聚,导致低氧性呼吸功能不全或衰竭。PAP被认为处于活动期的标准包括:(1)持续或进行性症状,如呼吸困难、咳嗽、咳痰、胸痛、体重减轻;(2)肺功能下降,如用力肺活量(FVC)或一氧化碳弥散量(DLCO)下降;(3)动脉血气测量的低氧血症(PaO2、SaO2、AaDO2);(4)高分辨率CT(HRCT)上新出现或恶化的PAP特征性浸润,包括但不限于磨玻璃影和铺路石征。排除其他原因或并发症,如呼吸道感染、肺栓塞、肺动脉高压和充血性心力衰竭等。
2008年研究人员提出了一种基于症状和PaO₂水平的疾病严重程度评分[2,7]。该评分易于计算,并已用于临床试验中的患者分层[8, 9]。后续提出的其他评分纳入了吸烟状态和HRCT表现,这些评分与预后相关性良好[10]。目前尚不清楚机会性感染应被视为疾病严重程度的指标,还是仅作为一种并发症[1]。PAP诊疗中心的意见有助于患者评估、确定疾病是否处于活动期以及明确管理方案。
PAP的疾病进展尚无标准定义,但普遍认为其表现为呼吸症状恶化、肺功能测试(FVC、DLCO)下降、呼吸衰竭的发生或恶化,包括需要氧疗,以及在排除其他原因后PAP相关CT表现的恶化。基于之前的观察性研究[11, 12, 13]和临床试验[8, 9],DLCO和AaDO2可能是疾病进展最敏感的指标[1,14]。由于数据不足,目前尚无明确的肺功能测试或血气参数下降的阈值来定义疾病进展。全肺灌洗治疗间隔时间的缩短也被用作疾病进展的评判指标[8]。疾病进展应始终通过HRCT确认,同时需要排除其他合并的肺部疾病。虽然发生率存在差异,但高达20%的PAP患者可能并发肺纤维化[15],这一表现应被视为疾病进展的重要征象。在这种情况下,可以暂时使用2022年ATS/ERS指南中的进行性肺纤维化(PPF)定义进一步评估疾病进展[16],但这些标准在PAP中的应用仍需验证。
五、推荐意见
所有问题的检索策略、PRISMA流程图、纳入研究、偏倚风险评估、荟萃分析、证据概况和证据到决策框架均可在原文在线附录中查阅。首先我们将围绕个体干预措施及其支持证据提出推荐意见,随后提出了PAP鉴别诊断的算法(图1)和aPAP治疗的分级方案(图2)。
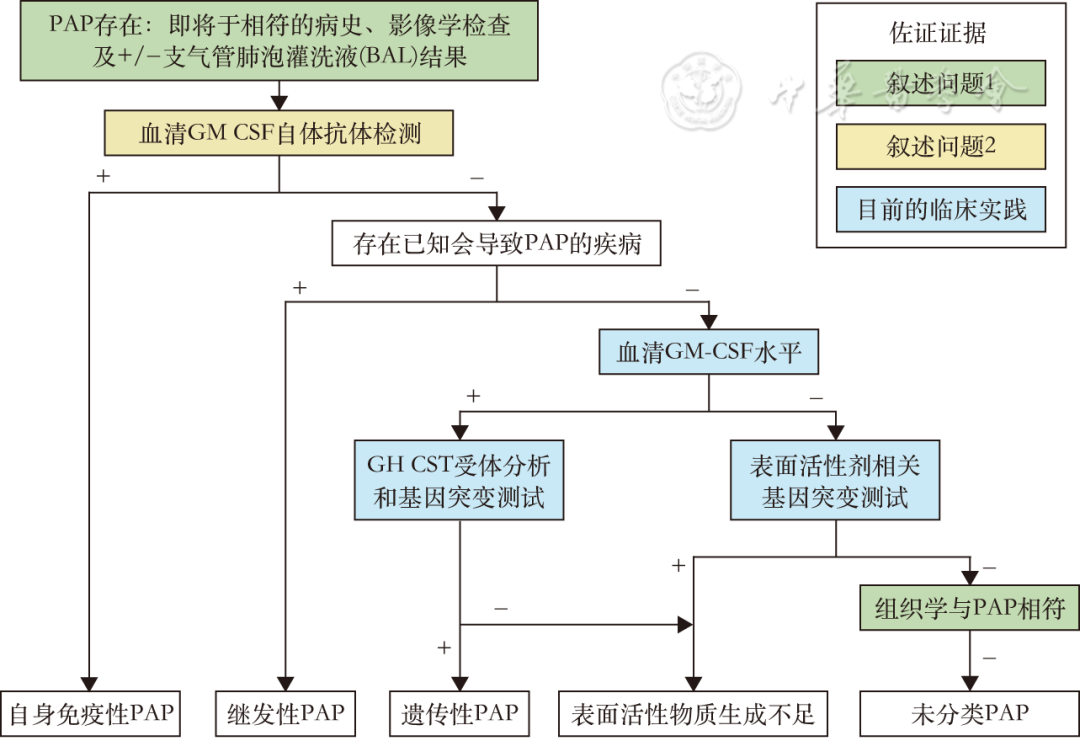
图1 肺泡蛋白沉积症(PAP)鉴别诊断的算法流程图
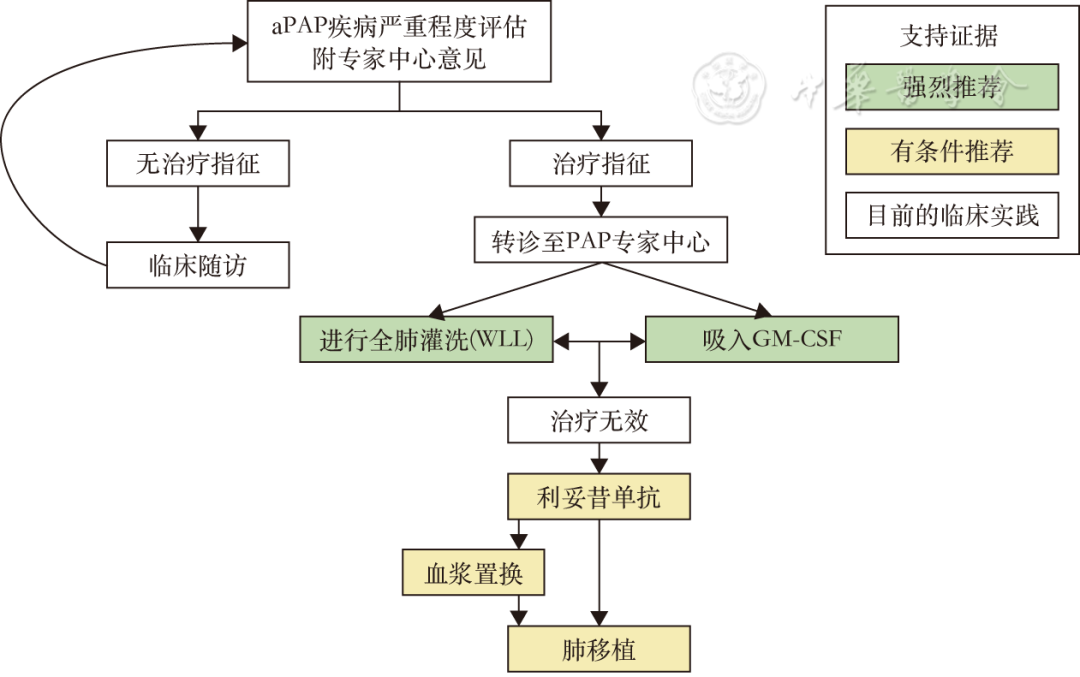
图2 自身免疫性PAP(aPAP)治疗的分级方案流程图
1. 推荐意见:我们推荐将进行BAL作为疑似PAP患者的诊断工作的一部分。BAL应包括细胞分类计数、PAS染色和微生物检查(强烈推荐,证据等级极低)。
2. 实际考虑:BAL可以做PAS染色和微生物学检查,这是一项简单技术,可在大多数开展支气管镜检查的医疗中心实施。患者代表更倾向于选择这种能够快速诊断、无需活检等更具创伤性干预措施的检查方法。
1. 推荐意见:我们建议不要常规地将进行肺活检作为疑似PAP患者诊断工作的一部分(有条件推荐,证据等级中等)。
2.实际考虑:肺活检是一种创伤性技术,可能因取样误差而无法诊断PAP,且存在已知的并发症风险和死亡风险[17]。部分医院无法提供肺活检服务。患者代表更倾向于选择能够快速诊断且无需更具创伤性干预措施的检测方法。若考虑进行肺活检,应基于获益/风险评估并与PAP诊疗中心协商,与患者讨论创伤最小术式的优势与局限性。
1. 推荐意见:我们推荐对所有疑似或已确认患有PAP综合征的患者进行GM-CSF抗体检测以诊断自身免疫性PAP(强烈推荐,证据等级中等)。具体证据总结见在线附录。
2. 实际考虑:确保进行恰当的检测以测定(而非仅定性检测)GM-CSF抗体滴度至关重要。仅凭抗体检测结果呈阳性或阴性不足以诊断自身免疫性PAP,应报告抗体浓度,且此类检测最好在具备丰富经验的实验室内完成(参见原文补充附录)。所有病例应转诊或与公认的PAP诊疗中心(见原文附录)讨论,以获得有关应在哪个实验室进行检测以及如何适当解释结果的建议,特别是在进行更具创伤性的检查之前。
1. 推荐意见:我们推荐对有气体交换障碍和症状或功能障碍证据的自身免疫性PAP患者进行双侧全肺灌洗(强烈推荐,证据等级极低)。由于缺乏证据,不能推荐或反对其他PAP类型的全肺灌洗。我们建议根据个体病例征询诊疗中心的意见。
2. 实际考虑:需要说明的是,PAP的治疗适应证应与具有全肺灌洗执行经验的公认PAP诊疗中心讨论,因为目前还没有全肺灌洗的标准化方案。从患者的角度来看,如果临床指征明确,全肺灌洗的主要优势在于,它可以作为一种独立治疗方式,恢复相对较快,且不需要每日用药。一些报道出的缺点包括需住院治疗、费用较高,且当附近无专业诊疗中心时患者可能需长途跋涉。此外,并非所有国家均可开展全肺灌洗,这限制了部分患者的可及性。全肺灌洗是一种创伤性程序,存在如发热、肺炎或气胸等并发症的风险。
1. 推荐意见:我们推荐对确诊为自身免疫性PAP且有症状的患者使用吸入性GM-CSF(强烈推荐,证据等级极低)。
2. 实际考虑:给予GM-CSF或可预防或延迟后续的WLL。WLL是一项昂贵的干预措施,需住院并在全身麻醉下进行。PAP患者常需定期接受WLL,有时甚至需每月一次。吸入GM-CSF若能长期维持疗效,则有望减少重复WLL的需求,从而降低相关治疗成本[18, 19, 20, 21, 22, 23]。在纳入的RCT中,与安慰剂组相比,GM-CSF组的严重不良事件并未更常见。因此,治疗可被认为是安全且无创的,我们相信其可接受性会很高。吸入GM-CSF治疗可能可以在家中或当地医疗机构进行,这增加了公平性。
1. 推荐意见:我们建议对确诊为自身免疫性PAP且在全肺灌洗治疗或外源性GM-CSF治疗后仍有症状、需要补充氧气的患者使用利妥昔单抗(有条件推荐,证据等级极低)。
2. 实际考虑:尽管利妥昔单抗在aPAP患者中的安全性尚未得到充分评估,但其他疾病领域有大量数据可供参考。更具体地说,Cochrane综述在评估利妥昔单抗治疗类风湿性关节炎时更详细地评估了成人使用类似剂量(两次静脉输注,每次1 000 mg,输注间隔为14 d)的安全性[24]。在48~56周随访或104周随访中,添加利妥昔单抗与严重不良事件的风险增加无关。利妥昔单抗在前6个月内因不良事件导致的停药率有增加趋势;这一趋势在1年随访时消失,并在更长的随访中逆转。在儿童中,一项评估利妥昔单抗治疗儿童激素依赖性肾病综合征的荟萃分析,更详细地评估了输注1~4次利妥昔单抗(375 mg/m2)的安全性。该荟萃分析未发现感染或心血管疾病事件风险增加,但发现输液反应风险有增加的趋势。作者报道,儿童严重过敏反应的发生率极低[25]。
1. 推荐意见:我们建议对确诊为自身免疫性PAP且在接受外源性GM-CSF和利妥昔单抗治疗后仍有症状、需要高流量氧疗(≥4 L/min)或1年内接受过2次或以上全肺灌洗的患者使用血浆置换。对于常规治疗无效的患者,也建议使用血浆置换(有条件推荐,证据等级极低)。
2. 实际考虑:血浆置换的安全性在Cochrane关于血浆置换治疗吉兰-巴雷综合征有效性的综述中进行了详细的评价[26]。基于三项试验共计556例受试者的数据,血浆置换未增加感染(RR=0.91,95%CI:0.73~1.13)、血压不稳定(RR=0.88,95%CI:0.64~1.22)、心律失常(RR=0.75,95%CI:0.56~1.00)或肺栓塞(RR=1.01,95%CI:0.26~4.00)的风险。然而,应注意的是,纳入的研究采用了2~6次血浆置换,比aPAP中建议的次数少。基于一项纳入>15 500例患者(主要为成人)[27]的系统综述(该综述包含了荟萃分析),血浆置换相关病死率估计为0.05%。一项叙述性综述总结了593例神经系统疾病儿童接受>4 500次血浆置换的并发症情况[28],结论是该干预措施耐受性良好,且相关不良事件可预见和避免。据报道,在所有接受血浆置换的单次治疗过程中有15%发生了并发症,在患儿群体中,有70%发生了并发症。然而,危及生命的并发症仅占治疗次数的0.4%和病例数的2.4%。患者代表认为,对于治疗无效且疾病负担严重的aPAP患者而言,潜在的全肺灌洗预防和缺氧改善可能是重要的。
1. 推荐意见:我们建议对尽管接受全肺灌洗和(或)药物治疗仍进展的PAP患者进行肺移植,且这些患者符合国际心肺移植协会(ISHLT)对间质性肺疾病患者的标准(有条件推荐,证据等级极低)。
2. 实际考虑:对于治疗无效的PAP,无论是否伴有肺纤维化且可能在几年内死亡,肺移植结合终身药物治疗和医疗监测是一种可以改善生活质量的选择[29]。事实上,即使无法保证延长生存期,仍有许多患者考虑肺移植以缓解症状和改善生活质量[29]。然而,仍有少数人拒绝移植并希望接受姑息治疗[30]。一项综述纳入了28项成人研究,并从医疗支付者的角度对肺移植的等候名单进行了成本效用评估,在至少10年的时间范围内,每质量调整生命年的成本为42 459~154 051美元[31]。终末期肺疾病和慢性呼吸功能不全患者的护理成本应与肺移植住院护理(包括手术和ICU住院费用)以及终身药物和护理费用的成本相平衡[31]。
对于尽管接受全肺灌洗和(或)药物治疗仍有病情进展的PAP患者,一个重要问题是评估供体肺PAP复发的风险。然而,目前尚不清楚疾病复发风险与PAP病因之间是否存在相关性。在自身免疫性PAP中,复发的风险存在,因为肺移植后可能持续产生GM-CSF自身抗体。这可能与器官移植后所需的免疫抑制治疗对自身免疫过程的潜在影响相平衡。在遗传性PAP中,移植肺中供体巨噬细胞被遗传性PAP患者的宿主巨噬细胞替代,可能增加供体肺中PAP复发的风险。幸运的是,数例肺移植后随访长达3.5年的病例报告了供体巨噬细胞在肺内的持续存在[32]。目前,移植肺上PAP复发的风险是一个难以解决的问题,但这并非肺移植的禁忌证。某些罕见的遗传性PAP(如CSF2RA或CSF2RB缺陷、OAS1缺陷等)如果肺部没有不可逆的纤维化损伤,可以通过骨髓移植治疗(详见补充附录)。对于由CSF2RA或CSF2RB基因突变引起的遗传性PAP以及尽管接受所有治疗仍进展的PAP,另一种理论上的可能性是考虑肺移植与骨髓移植联合治疗。
如前所述,治疗适用于疾病处于活动期或恶化的患者。治疗的适用性应基于肺功能受损程度、CT影像学变化、血氧饱和度水平和生活质量。如果不存在呼吸衰竭或危及生命的并发症,且患者的生活质量尚可,则可以采用观察等待策略。在对20家开展全肺灌洗的PAP诊疗中心的调查中,各中心的全肺灌洗适应证有所不同[20]。具体适应证包括肺功能不明原因下降、静息PaO2下降、基于连续胸部影像学比较的肺部疾病严重程度恶化、DLCO下降、FVC下降、脉搏血氧仪测量的静息血氧饱和度(SpO2)下降,或呼吸道症状加重。在aPAP吸入GM-CSF的随机对照试验(RCT)中,纳入标准在疾病活动性方面有所不同。在PAGE试验中,如果患者在仰卧位呼吸空气5 min后PaO22[8]。在IMPALA试验中,纳入标准为:基线评估前至少两个月内病情稳定或进展的aPAP、静息PaO24%,且AaDO2≥25 mmHg[9]。工作组认识到该领域需要更多研究,并需要就治疗适应证标准达成国际共识。aPAP治疗分级方案(图2)基于小组成员的共识:(1)PICO问题3~7中建议的强度,重点关注相应干预措施所需的潜在获益、风险和资源;(2)支持这些PICO的证据的确定性;(3)当前临床实践。
1. 治疗反应:目前尚无定义治疗反应的标准。PAP的治疗目标是实现疾病消退或长期疾病稳定,而无需重复进行全肺灌洗。在关于全肺灌洗疗效的报告中,血气参数的变化和影像学改善被用于评估治疗反应[20,33]。在GM-CSF的 RCT中,呼吸室内空气时的AaDO2被选为主要终点,而DLCO和HRCT浸润的改善被作为次要终点[8, 9]。这些及其他RCT结果的改善程度已由工作组审查,并在上述PICO问题2的证据总结中概述。在回顾性研究和吸入GM-CSF的RCT中,偶有报道PAP患者的生活质量和(或)症状的变化[8, 9],尽管这些研究依赖于对PAP非特异性的呼吸问卷。尽管一些循环生物标志物,如 KL-6、SP-D、LDH、YKL-40、肿瘤组织抗原[18, 19,34, 35, 36, 37, 38, 39],似乎有望用于评估治疗反应,但仍需验证研究。工作组认识到肺功能测试和血气参数在定义治疗反应中的实用性,但未指明具体的下降或改善阈值。除了功能评估外,建议在适当的随访期(至少 6 个月)内仔细评估症状和影像学变化。
2. 难治性疾病:难治性PAP可定义为尽管进行了充分治疗和适当随访(约6个月),但呼吸道症状、肺功能或气体交换受损以及HRCT浸润持续或恶化。应排除术后并发症作为治疗失败的原因。随着时间的推移需要重复全肺灌洗以及两次连续全肺灌洗之间时间间隔的缩短已被用作治疗无反应的指标[9,40],但这些研究异质性太大,无法得出结论。循环和遗传生物标志物也存在同样的情况[41]。专家组建议在治疗后对患者进行严密监测和全面评估,旨在判断疾病活动性,并排查治疗失败是否由短期或长期治疗并发症、或合并症所导致。
PAP的诊断和管理具有挑战性。要找到合适的治疗方法,首先需要区分引起PAP的不同疾病类型,但目前还缺乏标准化的诊断流程。本指南推荐使用BAL而非肺活检,来确认临床和影像学怀疑的PAP。本指南认为GM-CSF自身抗体检测是诊断aPAP最敏感和特异的检查。如果GM-CSF自身抗体浓度不足以引起PAP,则需要进一步的诊断测试来评估GM-CSF信号传导,例如使用中性粒细胞流式细胞术,或检测潜在的基因突变[1]。由于除aPAP外,PAP的病因具有异质性,因此当前指南不对其他形式的单一诊断试验提出具体建议。尽管如此,本指南建议及时将无法明确分类的PAP患者及时转诊至专业诊疗中心,以免延误诊断和治疗。在疾病结局方面,约7%的PAP患者会自发缓解且无需治疗[1]。在本指南中,我们建议在出现呼吸衰竭、肺功能受损或导致生活质量下降的症状时对患者进行治疗。尽管越来越多的证据支持DLCO、HRCT浸润和血气参数作为治疗指标,但专家组强烈建议应同时考虑多个方面,包括患者需求。这一概念在诊疗中心的临床实践中已被广泛接受[41]。对于大多数PAP患者,全肺灌洗治疗可迅速改善症状、气体交换和影像学表现[42]。然而,由于数据的缺乏,无法就全肺灌洗的长期影响得出结论[43]。同样,由于缺乏针对PAP患者的验证工具,治疗有效性(尤其是与生活质量相关的)证据较弱[41]。由于大多数研究都集中在成人疾病上[20,44, 45],专家组能够对成人aPAP患者的全肺灌洗提出积极推荐。尽管如此,基于小型且多为单中心的观察性研究或病例系列,专家组也对儿童PAP的管理提出了特别注意事项。
吸入GM-CSF是唯一在成人aPAP患者随机对照试验中研究过的治疗方法,获得了强推荐,但证据等级极低。由于终点和试验设计的异质性,目前无法对莫格司亭和沙格司亭进行直接比较[8, 9]。为了全面起见,我们提到吸入用沙格司亭(250 μg)最近已在日本获批用于治疗aPAP[46]。除了需要更多关于吸入GM-CSF疗效的长期数据外,专家组强调目前仍需关注PAP特异性疗效终点以及进一步标准化给药方案,以满足临床常规治疗以及未来临床试验。尽管最近的一项试验[44]探讨了是否应将WLL和吸入GM-CSF整合成特定的附加或序贯给药方案,但这一问题仍有待未来研究解答。
指南专家组强调,尽管部分建议所依据的证据质量较低,但基于所研究干预措施的实际效果和可行性,他们仍对几个关键问题做出了强推荐。本指南有几个局限性。首先,本指南提供的诊断建议指的是所有程序或测试均可用的理想情况,但能够提供GM-CSF抗体检测、GM-CSF信号传导评估或基因检测的中心很少,因此尽早转诊至PAP诊疗表中心或网络是必要的。其次,尽管专家组努力界定了疾病严重程度、进展标准及治疗指征,但这些定义主要仍依赖于个案分析和专家经验。第三,观察性研究和RCT中对治疗反应的测量方法仍然存在较强的异质性,亟须就具有临床意义的结果和最佳终点达成共识。第四,本指南提供的治疗分级(图2)应在个体层面考虑,治疗决策取决于多种因素,包括当地的可用性和报销政策。最后,本指南未对支持性治疗提出具体建议,如吸氧或肺康复。总之,指南专家组根据当前证据和临床经验,在信息充分的领域提出了知情建议。尽管在理解PAP综合征的发病机制和临床进展方面取得了巨大进展,但许多问题仍未得到解答;工作组提出了未来研究的若干建议。显然,许多研究主题需要国际合作,例如共识报告和国际注册。
本ERS指南基于全面系统的文献综述制定,该综述梳理了当时可用的相关已发表证据。专家组鼓励卫生专业人员在临床实践中参考本指南。然而,本指南提出的建议可能并不适用于所有情况。卫生专业人员有责任咨询其他相关信息来源,根据每位患者的健康状况并在适当时与患者及其护理人员协商,做出适当和准确的决定,并在开具处方时遵循适用于药物和器械的当地或国家法规。
本文件于2024年4月16日由ERS执行委员会批准。
参考文献(略)

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)