医脉通编译整理,未经授权请勿转载。
家族性高胆固醇血症(FH)是一种常
目前已经开发了几种工具和筛查策略来帮助临床医生尽早诊断和治疗。随着电子病历(EMR)的广泛使用,现在可以通过人工智能和机器学习算法来识别可能患有FH的患者,提供更好的患病率估算数据。本文将概述FH的遗传学、临床表现、检测策略以及当前基于指南的治疗方法。
基因突变和患病率
家族性高胆固醇血症最主要的突变涉及低密度脂蛋白受体(LDLR)基因,可导致代谢LDL-C的LDLR受体缺乏。不常见的突变包括与LDLR相互作用的分子存在突变,例如载脂蛋白B(apoB)或PCSK9等,也可以导致血浆LDL-C升高(图1)。
FH包括杂合子型(HeFH)和纯合子型(HoFH),根据大型遗传研究,前者的患病率估计为1/220,后者的患病率估计为1/300,000。HoFH患者可在30岁之前出现心血管事件,临床表现更为严重,预后也更差。
HeFH和HoFH的患病率可能因种族而异。男性和女性患病率相似,但男性可能比女性更早发生心血管事件。
临床表现
通常,FH患者从小就会出现LDL-C升高,因此会表现为早发心血管疾病。研究表明,与未患病儿童相比,FH患儿8岁时颈动脉内膜厚度更大。另有研究表明,高达25%的FH青少年患有冠状动脉钙化。
在人群水平,FH患者的动脉粥样硬化性疾病患病率至少是非FH患者的3倍。在HoFH患者中,动脉粥样硬化性心血管疾病的进程加速,在30岁之前可能就已经发生了第一次心血管事件。
目前已经开发了几种临床标准来帮助FH的临床诊断,均围绕LDL-C水平、家族史和体格检查结果来进行。LDL-C≥190 mg/dL即可怀疑FH,若水平更低但同时有家族史和/或体格检查结果,仍可诊断。家族史主要是指一级亲属有早发心血管事件(男性<55岁,女性<65岁)。
体格检查结果包括黄色瘤(图1)和角膜弓(图2)。
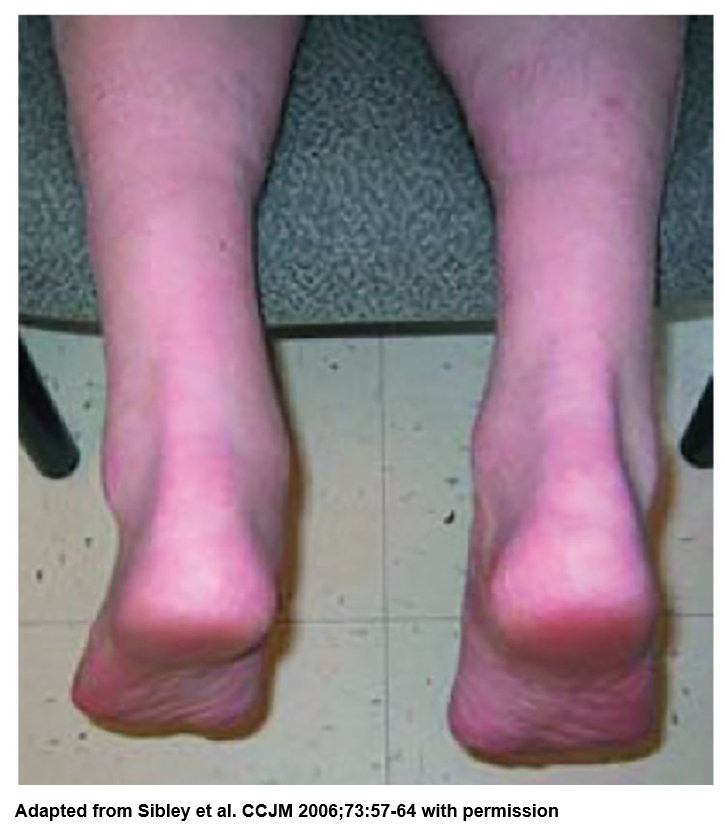
图1 跟腱黄瘤

图2 角膜弓
诊断和筛查策略
荷兰血脂网络标准(DLCN)是诊断FH使用最广泛的临床评分系统之一,根据血脂水平、体格检查、家族史和遗传数据(如果可用)得出分数,高于8分诊断为“确定的FH”。
表1 诊断家族性高胆固醇血症的DLCN标准

注:DLCN为荷兰临床脂质网络标准;分值>8分为确诊家族性高胆固醇血症(FH)、6~8分为FH可能性大,3~5分为可能的FH;LDL-C为低密度脂蛋白胆固醇,LDLR为低密度脂蛋白受体,Apo B为载脂蛋白B
根据该标准,判定为“确定的FH”的患者接受基因检测时,突变检测率为30%-40%。这表明,可能并非所有的突变都经过测试,多基因因素可能被忽略了。因此,对于建立诊断和合理治疗来说,表型可能比基因型更重要。国际动脉粥样硬化学会也认可了这一观点,该学会在FH的诊断中高度重视LDL-C水平和亚临床疾病。
那么,问题来了,基因检测的作用是什么?基因检测被认为是FH的金标准。一些研究表明,在任何LDL-C水平下,基因阳性的人患心血管疾病的风险均要高于基因阴性的人。基因检测还能解释表型异质性,因为某些突变与高风险相关。
另外,基因检测对治疗策略的选择也是有帮助的。比如HoFH患者完全没有LDLR,这种情况下他汀类药物治疗是无效的,需要调整治疗策略。而且,基因检测存在一些障碍,例如成本、隐私等问题。此外,如果有强有力的表型证据,没有发现基因突变也不能排除诊断。
欧洲的数据表明,10年内识别9,000例FH患者可以预防847例冠心病,203例冠心病死亡,并可以增加767个质量调整生命年。
基于指南的治疗
降低LDL-C水平是主要的治疗目标之一。一线治疗为最大耐受剂量的他汀,应尽早开始,尤其是当LDL-C mg/dL时。在一级预防时,目标LDL-C通常为100 mg/dL,但越低越好;二级预防时,目标值应小于70 mg/dL。如果单用他汀不能达标,可加用
同时,进行生活方式干预以改变其他危险因素也是必不可少的。通过生活方式干预可以适度降低LDL-C水平。
对于HoFH患者或其他药物治疗无反应的患者,可考虑进行LDL血液分离术。其他疗法,包括
文献索引:Nishant Shah. Familial Hypercholesterolemia: Early Diagnosis and Treatment is Key for Cardiovascular Prevention. ACC. Apr 16, 2020.
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)