
近年来,基于肠促
2026年4月29日,发表于国际权威期刊《自然》(Nature)的一项临床前研究,向我们展示了全球首款靶向GLP-1R、GIPR及PPARα/γ/δ的单分子5重受体激动剂(GLP-1-GIP-Lani)的最新研究进展。

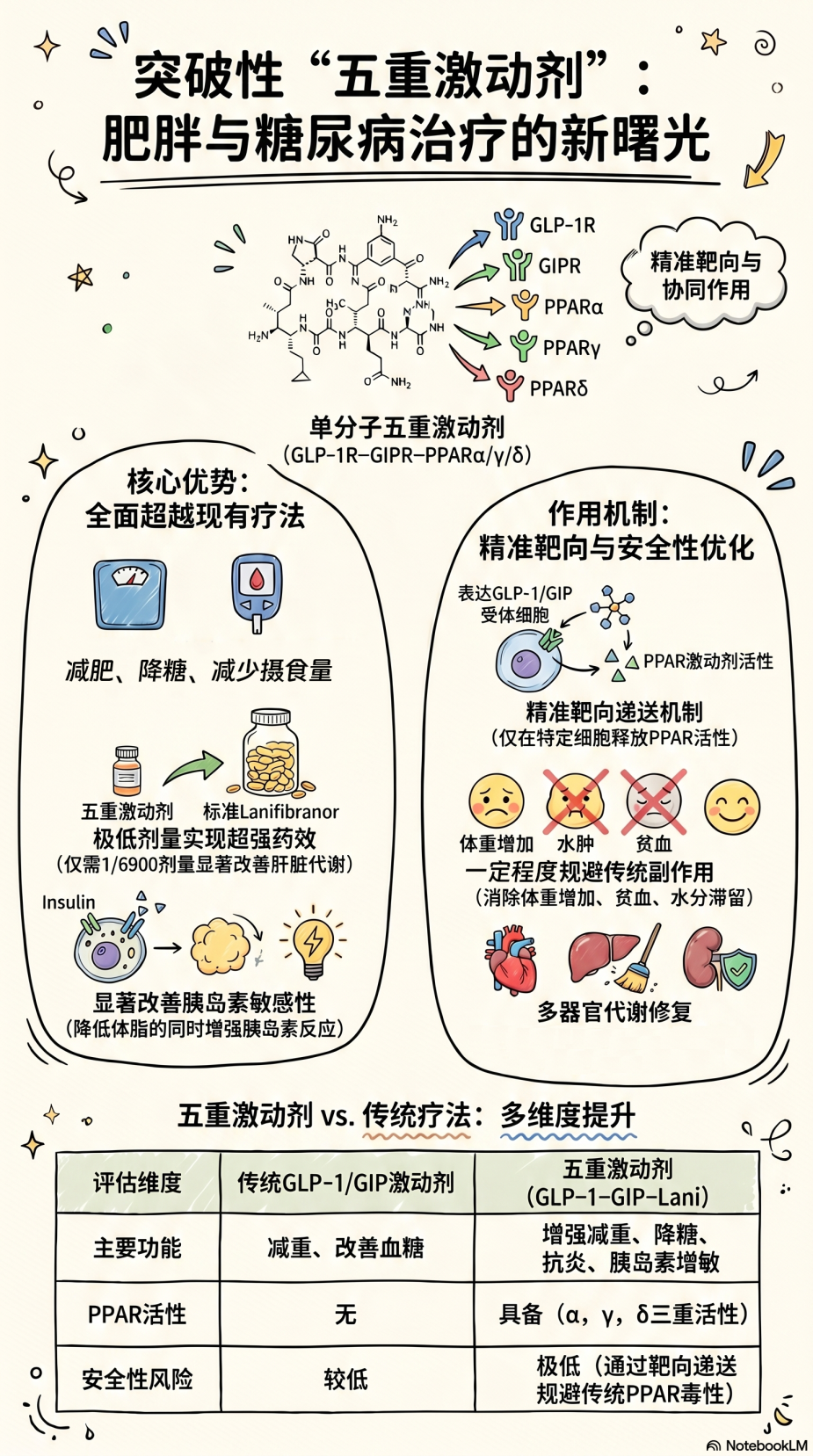
这款创新药物巧妙地结合了两项经典靶点(GLP-1、GIP)与强大的三靶点“代谢修复分子”(PPAR α、γ、δ),不仅在动物模型中展现出显著的减重与降糖潜力,更通过独创的“精准递送”技术,很大程度上规避了传统减重药的副作用风险。


大家熟知的单靶点减重药物,其实只瞄准了体内1个叫 GLP-1 的靶点;这就相当于只派了1名专家去帮你控制食欲。后来的双靶点减重药,同时瞄准了2个靶点(GLP-1和GIP),2名专家协同作战,效果自然更好。
这一次,科学家有了更大胆的想法:他们在2名“老将”的基础上,又拉来了一个代号为 Lani 的“三人专家团”——即调节脂肪和代谢的三个关键核受体:PPAR α、γ 和 δ。
2名老将 + 3人专家团 = 5个靶点同时开工! 它们不仅能有效管住嘴,还能深入细胞内部,疯狂燃烧脂肪并全方位修复代谢。
新加入的“三人专家团(Lani)”本来是一款处于临床3期的强效老药,在治疗
这项研究最绝妙的突破,就是给 Lani 戴上了“GPS导航”。
科学家利用巧妙的化学技术,把这个容易惹祸的 Lani 牢牢绑在了前面的2名“老将”身上。由于“老将”自带导航,只会进入特定的目标细胞,这就好比把强效药装进了“定向快递箱”,实现了精准投递,绝不波及无辜组织。
正因为投递极其精准,新药现在的有效剂量仅为原来的将近七千分之一(确切地说是缩小了6898倍)。这不仅完美避开了全身广泛用药的毒副作用,还激发出极其强大的威力。


在饮食诱导肥胖(DIO)的小鼠模型中,GLP-1-GIP-Lani展现出突破现有机制“天花板”的代谢调节效能。
在低至10 nmol/kg的日剂量下,该5重受体激动剂在降低体重、减少脂肪组织量及抑制摄食方面,呈现出显著优于单纯双靶点激动剂的效能。机制研究表明,该药物能进入中枢神经系统,并通过增强下丘脑阿黑皮素原(POMC)神经元的活性来进一步抑制食欲。
在葡萄糖稳态调节方面,GLP-1-GIP-Lani显著改善了全身胰岛素敏感性与葡萄糖耐量。高胰岛素-正糖钳夹试验与分子层面的分析显示,该药物能够强效抑制肝脏内源性葡萄糖的生成,并显著下调糖异生关键调节酶(Pcx 和 Pepck1)的基因表达。此外,该药物还显著促进了棕色脂肪组织(BAT)、骨骼肌、肝脏及心脏等关键代谢靶器官的组织特异性葡萄糖摄取。


克服系统性毒副作用是该药物最具转化潜力的突破之一。长期给药证实,该5重受体激动剂并未引发传统PPAR激动剂典型的心脏肥大、体重反弹、体液潴留或贫血等不良反应,也未对肾脏系统产生显著毒性。在保证高安全性的同时,该药物表现出显著的脏器保护多效性:
肝脏抗炎与脂质清除: 转录组学分析表明,GLP-1-GIP-Lani在肝脏及骨骼肌中强烈诱导了抗炎基因程序的表达。相较于双靶点激动剂,它更有效地降低了肝脏甘油三酯水平,并逆转了肝脏的炎症状态。
心血管血流动力学改善: 在心血管功能评估中,该药物未引起血压异常,反而降低了静息心率,并进一步改善了心脏性能,包括显著提升左心室射血分数、缩短分数、心输出量及每搏输出量。
能量稳态安全性界限: 在针对正常体型(非肥胖)小鼠的安全性测试中,该药物并未诱发异常的体重减轻、低血糖或血脂紊乱,证实其具有良好的代谢稳态调节安全性。


GLP-1–GIP–Lani单分子5重受体激动剂的问世,标志着代谢疾病多靶点协同治疗在机制层面的一次重大飞跃。它通过首创的“靶向递送”策略,成功将强效的核受体代谢修复药物精准送达至目标细胞,在打破现有减重与降糖疗效极限的同时,完美跨越了传统药物的副作用鸿沟。虽然该药物目前仍处于临床前研究阶段,但这一医学黑科技无疑为未来攻克
参考文献
本视频/资讯/文章的内容不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。医脉通是专业的在线医生平台,“感知世界医学
