一年一度的美国血液学会(ASH)年会如期而至,作为全球血液学领域的顶尖学术盛会,今年依旧星光璀璨、干货满满。新一代 BCL-2 抑制剂(BCL-2i)索托克拉(BGB-11417)凭借血液肿瘤领域的强大治疗潜力,持续成为学界关注焦点。本次 ASH 会议首次口头报道了索托克拉联合
伴t(11;14)的多发性骨髓瘤(MM)约占MM患者的15-20%,是一种具有独特特征的疾病亚群,且在蛋白酶体抑制剂(PI)、免疫调节药物(IMiD)、抗CD38单克隆抗体时代并未显著改善t(11;14)MM患者的缓解率和预后6。
BCL-2i在该类患者中显示有效,然而目前尚无任何BCL-2靶向疗法被批准用于治疗MM。BCL-2i联合地塞米松或卡非佐米促进BCL-2依赖性,可能进一步增强MM治疗效果;索托克拉是新一代BCL2i,与
BGB-11417-105(NCT04973605)研究中,既往索托克拉(320mg/640mg)+地塞米松两药方案治疗中位3线经治t(11;14) R/R MM患者耐受性良好,并诱导了深度持久的反应,总体ORR为78.2%,≥CR率为21.8%,其中640mg队列的中位无进展生存期(PFS)为12.9 个月2。
本文最新公布索托克拉+卡非佐米(K) + 地塞米松剂量递增队列的初步结果。
研究类型:BGB-11417-105为开放标签、1b/2期剂量递增和扩展研究。主要评估索托克拉治疗t(11;14) R/R MM耐受性和抗肿瘤活性。此为索托克拉+卡非佐米+地塞米松剂量递增队列的初步结果。
入组标准:确诊的t(11;14) R/R MM患者;既往接受过≥3线治疗,包括PI、IMIDs和抗CD38抗体(部分地区患者不需要既往接受抗CD38抗体);无已批准的其他方案可用。
治疗方案:索托克拉(Sonro, 320 mg qd或640 mg qd) +地塞米松 (Dex, 40mg qw)+卡非佐米(56 mg/m2 [K56]或70 mg/m2 [K70],d1,8,15)治疗,直至疾病进展或出现不可接受的毒性。
研究终点:按照NCI-CTCAE v5.0标准判定的安全性,研究者判定的总缓解率(ORR)。

图1 研究设计
1.基线
截至2025年9月3日,共纳入22例患者,其中Sonro 320 mg+ K56+Dex, Sonro 320 mg+ K70+Dex分别为11例和7例,Sonro 640 mg+ K56+Dex 4例,正在入组中。所有患者中位年龄为65岁(范围,44-77岁),73%为男性;中位既往治疗线数为4(范围,2-8线),既往≥4线治疗比例为64%;三类药暴露比例为86%,三类药难治性比例为41%。
表1 基线数据
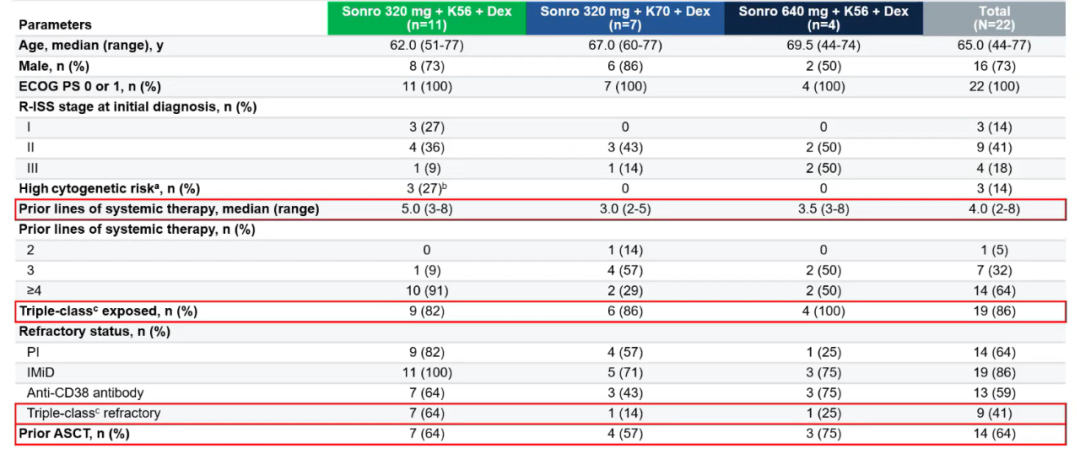
2.疗效
22例患者疗效可评估,中位随访10.4个月,总体患者ORR为86% (95% CI, 64%-97%),其中完全缓解/严格完全缓解(CR/sCR)率为38% (95% CI, 18%-62%)。Sonro 320mg+K56+Dex, Sonro 320mg+K70+Dex, Sonro 640mg+K56+Dex 中位随访分别为16.4个月,9.1个月,和5.4个月,ORR率分别为82%,86%和100%,CR/sCR率分别为36%,57%和0%。
至缓解的中位时间大约为1.0个月,不同剂量组间一致。
中位随访10.4个月(范围2.6-25.8),中位缓解持续时间(DOR)和中位PFS未达到;12个月DOR率为80.4%(95% CI, 50.6-93.2%),6个月PFS率为69.3%(95% CI, 43.7-85.0%)
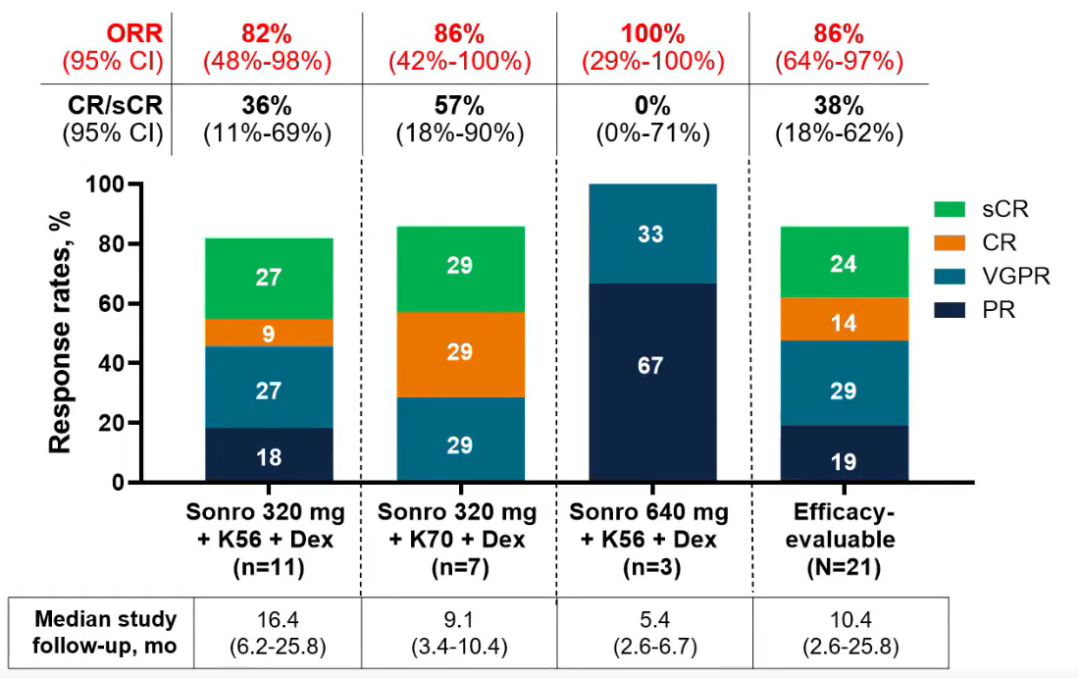
图2 缓解率
3.安全性
1)安全性可管理:未发生导致死亡的TEAE;索托克拉停药或减量罕见,各发生1例;截至目前未达到最大耐受剂量(MTD);所有剂量水平下,未发生心衰,心梗或心脏骤停事件。
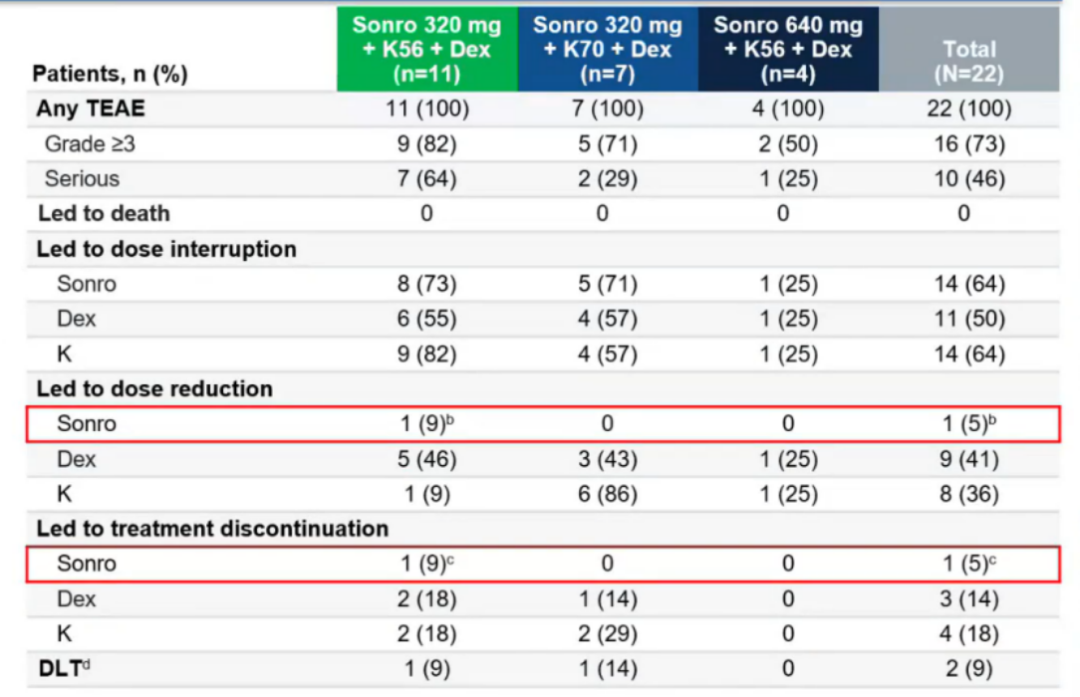
图3 安全性
2)整体耐受性良好:最常见的治疗期间出现的不良事件(TEAE)包括疲劳(50%)、失眠(41%)、恶心(36%)、贫血(32%)和背痛(27%)等;大部分为1-2级且表现为短暂性。
3)安全性特征与单个研究药物已知的安全性特征一致:任何级别血液学TEAE发生率55%,≥3级血液学TEAE发生率为36%,≥3级中性粒细胞减少症发生率为14%;≥3级感染发生率为23%。
索托克拉+卡非佐米+地塞米松联合治疗多线经治的t(11;14)R/R MM患者,显示出可耐受的安全性,尚未达到最大耐受剂量,未发生导致死亡TEAE,且索托克拉减量和停药事件罕见;
该三药方案获得令人鼓舞的抗骨髓瘤活性,ORR为86%,CR/sCR率为38%,中位随访10.2个月,中位PFS和DOR未达;
BGB-11417-105研究尚在入组,且不同联合方案也在评估中。
路瑾教授
t(11;14)易位约见于15%-20%的新诊断患者2和24.7-27%的R/RMM 4-5。此外t(11;14)MM趋向于寡分泌型,M峰较小,循环浆细胞数量较多,倾向于只产生IgG λ或轻链3。尽管目前多数指南仍将其划分为标危因素,但研究发现,携带t(11;14)的MM患者在PI、IMIDs、抗CD38单克隆抗体时代并未显著改善缓解率和预后6,且其疾病特征(如缓解速度慢、缓解深度不足)也颇具独特性7-8,这提示t(11;14)的预后影响可能比以往认知的更复杂,值得临床给予更多关注。
既往研究表明t(11;14)浆细胞具有对BCL-2依赖性的独特生物学特征,且对BCL-2i(如维奈克拉)表现出较高的敏感性9。临床研究也验证BCL-2i单药或联合方案治疗t(11;14) R/RMM患者均有突出疗效10-14,19。如维奈克联合地塞米松的两药方案治疗中位3线和5线经治t(11;14)R/RMM,ORR分别为60%和48%,≥VGPR 30%和36%,≥CR率 5%和7%,TTP分别为12.4和10.8个月11。维奈克拉联合卡非佐米三药方案(VenKd)治疗中位2线经治t(11;14) RRMM,ORR为92%,≥CR率为22%,中位PFS分别为32.2个月(Ven 400mg)和42.4个月(Ven 800mg)。此外维奈克拉联合达雷妥尤单抗三药方案(VenDd,Ven 400mg/800mg) 较DVd治疗中位1线经治t(11;14) R/RMM患者,达更深缓解和更长PFS,ORR分别为96%和65%,≥VGPR率93%和39%,≥CR率67%和19%, 33个月PFS率分别为73.4% 和38.8%15-16。故此,国内外指南均推荐BCL-2i用于R/RMM伴t(11;14)患者,其中NCCN指南推荐维奈克拉/地塞米松联合达雷妥尤单抗或PI方案17-18。
二代BCL-2i索托克拉,相较一代BCL-2i,具有对BCL-2蛋白更强的抑制作用以及更高的选择性19, 在临床研究中也表现出令人鼓舞的早期疗效。BGB-11417-105研究中索托克拉320mg/640mg联合地塞米松的两药方案治疗中位3线经治t(11;14) R/RMM患者,ORR为73.7%/80.6%,≥CR率为15.8%/25.0%,DOR 未达/12.2个月,中位PFS为6.6个月/12.9个月2。本研究中,进一步联合卡非佐米的三药方案治疗中位4线经治t(11;14) R/RMM患者,中位随访10.4个月,ORR为86%,≥CR率为38%,DOR和PFS未达,至缓解的中位时间大约为1.0个月2,总体展现深度持久缓解的潜力。
目前BGB-11417-105研究仍在进行中,更多联合方案正在探索。索托克拉联合卡非佐米与地塞米松的初步数据,为t(11;14)阳性RRMM患者带来了令人鼓舞的深度缓解与可控安全性。未来结果值得期待,或将为t(11;14)R/RMM患者开辟精准治疗新路径。



路瑾 教授
主任医师 教授 博士生导师
北京大学人民医院,北京大学血液病研究所
主要进行多发性骨髓瘤、原发系统性淀粉样变性、淋巴瘤、细胞免疫治疗等的临床以及实验室的研究。
中国医师协会血液科医师分会副会长、总干事
北京医师协会血液医师分会会长
北京市血液病质控中心主任
中国医师协会多发性骨髓瘤专业委员会副主任委员兼组织细胞疾病专业委员会副主任委员
中国老年医学会血液病学分会副会长兼多发性骨髓瘤学术委员会主任委员
中华医学会血液学分会浆细胞学组副组长
中国女医师协会血液病专业委员会多发性骨髓瘤及相关疾病专业学组副组长
CSCO骨髓瘤专家委员会副主任委员
国际原发系统性淀粉样变性协作组成员、国际骨髓瘤工作组、亚太骨髓瘤工作组委员、国际肾脏与单克隆免疫球蛋白病研究组委员
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)