elafibranor长期治疗使PBC患者的生化和症状改善至少3年
(5016)
Elafibranor(ELA)是一种PPARα/PPARδ激动剂,基于III期ELATIVE试验结果,已被FDA批准作为PBC患者的二线治疗。本研究报道了正在进行的ELATIVE开放标签扩展研究(OLE)中接受ELA治疗超过3年的研究结果。
完成ELATIVE双盲期(DBP)的患者可进入OLE研究,每日接受ELA 80 mg治疗。在DBP期间接受安慰剂(PBO)的患者,基线设定为首次OLE ELA给药前的最后一个非缺失值;对于在DBP期间接受ELA治疗的患者,基线则为DBP开始时。终点指标包括生化应答(碱性磷酸酶[ALP]<1.67×正常值上限[ULN],且较基线降低≥15%,以及总胆红素[TB]≤ ULN)、ALP正常化,以及ALP、TB、白蛋白、γ-谷氨酰转移酶(GGT)、
在DBP数据截止时,153例患者接受了ELA治疗,108例在DBP期间接受ELA,45例接受PBO。138例患者进入OLE研究,截至2025年5月仍有115例患者继续参与。治疗至第182周(W182)时,生化应答率维持稳定(W182:72.1%;31/43)。ALP恢复正常比例保持稳定(W182:18.6%;8/43)。ELA治疗对ALP的改善在W4即显现,并在由PBO转入的患者中具有持续性和可重复性;在W52之后的所有时间点,超过60%的患者ALP较基线降低≥40%(W182:67.4%;ALP平均变化:−47.1%)。肝功能标志物包括TB(Figure A)和白蛋白保持稳定;GGT和ALT水平下降。纤维化标志物(LSM和ELF)在ELA治疗期间保持稳定。
在基线存在中至重度疲劳的患者中(n=25),PROMIS T评分在W4即见改善,并持续至W156(均值[标准差] −8.5 [10.3]);在基线存在中至重度瘙痒的患者中也观察到类似结果(WI NRS评分,n=23;均值[标准差] −4.1 [2.3])。未发现新的安全性信号;未观察到新发横纹肌溶解、肌痛或治疗相关肌酸磷酸激酶(CPK)升高的病例。
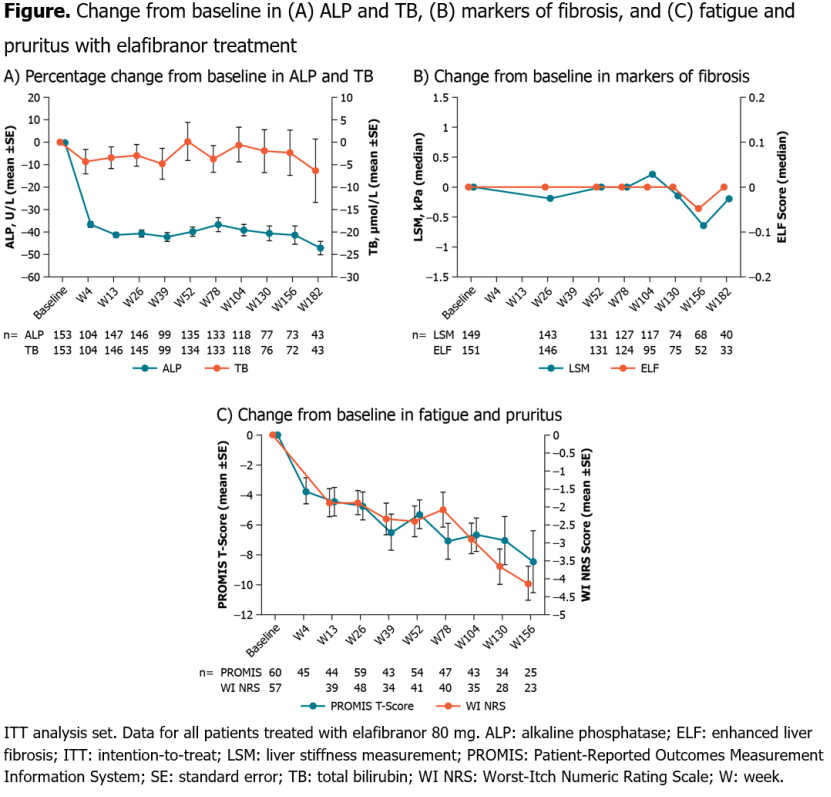
在正在进行的ELATIVE OLE研究中,ELA在胆汁淤积和纤维化生物标志物方面产生了快速、持续且可重复的应答,提示其具有延缓疾病进展的潜力。对胆汁淤积的积极影响、瘙痒和疲劳的持续改善、纤维化标志物的稳定以及一致的安全性特征,均证实了ELA适用于PBC的长期治疗。
基于ASSURE研究纵向瞬时弹性成像检测的疾病控制证据:Seladelpar治疗36个月与PBC患者肝硬度稳定或改善相关
(5031)
Seladelpar是一种选择性过氧化物酶体增殖物激活受体δ(PPARδ)激动剂,适用于与熊去氧胆酸(UDCA)联合治疗对UDCA应答不佳的PBC成人患者,或用于对UDCA不耐受患者的单药治疗。尽管Seladelpar改善胆汁淤积标志物的疗效已得到充分证实,但其对肝脏硬度值(LSM)的影响仍尚未充分探索,而LSM在PBC中通常随时间推移而加重。本研究在正在进行的 3 期开放标签 ASSURE 研究(NCT03301506)中期分析中,报告了接受 Seladelpar 治疗长达 36个月患者的纵向LSM数据。
研究纳入了来自安慰剂对照III期RESPONSE试验或早期Seladelpar研究的患者。采用振动控制瞬时弹性成像(FibroScan)评估 LSM,作为探索性终点。本分析纳入具有≥1次基线后LSM测量值的患者,排除经确认的IQR/LSM比值>30%的数值。以 Seladelpar 开始治疗时为基线,按基线LSM分层:<10.7、≥10.7且<16.9、以及≥16.9 kPa。评估12个月、24个月、36个月时的LSM变化,以及 36 个月时的分层类别变化。由于LSM值呈非正态分布,报告采用中位数。数据截止日期:2025年1月31日。
共 311 例患者纳入分析,获得114例患者36个月时的LSM值。总体基线中位(IQR)LSM为7.5(5.9,11.1)kPa。LSM中位变化为−0.2(−1.7,1.8)kPa,百分比变化为−2.9%(−22.8%,25.9%)。在基线LSM<10.7 kPa、≥10.7且<16.9 kPa、或≥16.9 kPa患者中,LSM至36个月时中位变化分别为+0.1(−1.3,1.8)kPa、−0.9(−3.6,4.8)kPa和−5.2(−10.6,2.4)kPa(图A)。同样,相对于基线中位百分比变化分别为+2.0%(−18.3,26.1)、−7.4%(−29.5,38.7)和−29.7%(−51.5,12.7)。分层类别变化方面,大多数患者(97/114 [85%])在36个月时保持稳定或改善(图B)。LSM较基线恶化≥30%的患者年龄更小(P<0.05),其他特征无显著差异。
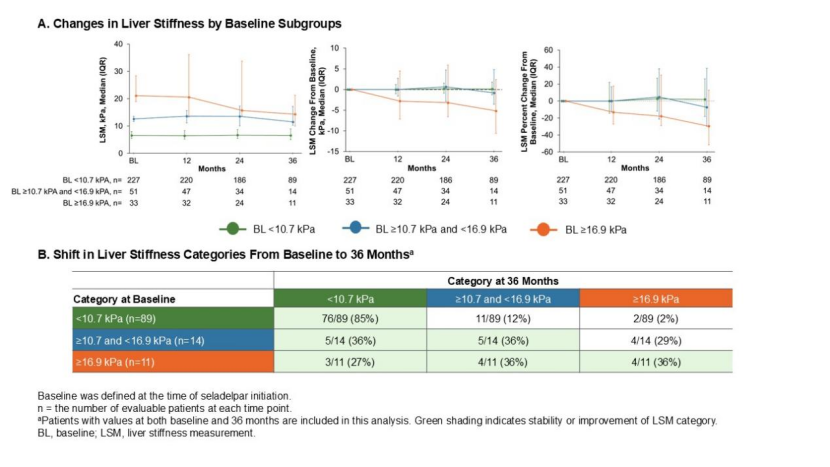
这项中期分析显示,大多数患者接受 Seladelpar 治疗 36 个月期间维持或改善了LSM分层类别。在疾病进展高风险人群(≥16.9 kPa)中,Seladelpar 治疗呈改善趋势。
CNP-104通过改善复合生化标志物和预后评分,展现PBC临床获益
(4399)
PBC是一种进行性自身免疫性肝病,存在显著未满足的临床需求,尤其是对40%的一线UDCA治疗应答不佳的患者。目前针对胆汁酸代谢的疗法无法解决潜在自身免疫发病机制,为新型免疫疗法提供了研发契机。为此,封装PDC-E2抗原的CNP-104纳米颗粒被设计用于重建PDC-E2免疫耐受,为PBC的疾病修饰提供了机制独特的治疗途径。本研究旨在探讨CNP-104对经验证的预后评估工具的影响,包括UK-PBC评分(肝脏相关结局)、GLOBE评分(无
在这项随机、安慰剂对照临床试验中,41例生化应答不佳(ALP >1.5×ULN)的PBC患者间隔一周接受了两次CNP-104或安慰剂给药。本文显示4 mg/kg CNP-104组(n=11)和安慰剂组(n=16)。研究评估了其安全性(既往已报道)及探索性临床终点,包括UK-PBC 5年风险评分、GLOBE评分和ALBI评分(增幅<0.065分)。
CNP-104在各预后指标中均显示一致的获益。与安慰剂相比,CNP-104治疗组UK-PBC 5年风险评分存在组间差异(Δ−3.51% ,p = 0.010)。对ALBI评分(定义为6个月内变化≤0.065分)的探索性分析显示CNP-104 组应答率为 80%(8/10 例),显著高于安慰剂组的 26.7%(4/15 例)(P=0.0154)。已广泛应用的 GLOBE 评分显示两组间存在差异,安慰剂组评分恶化更明显(Δ 0.227,p = 0.0125),提示 CNP-104 可降低患者长期风险。
CNP-104可改善UK-PBC和GLOBE评分(长期风险降低的指标),在治疗难治性PBC人群中凸显其改变疾病进程的潜力。值得注意的是,这些获益在两次负荷剂量后即可观察到,为IIb期临床试验中慢性给药方案的进一步评估提供了依据。CNP-104 为 PBC 患者提供了一种多维度治疗策略,需要进一步进行验证性研究。
参考文献:
1. Cynthia Levy,Ulus Akarca,Mario Reis Alvares-daSilva,et al.LONG-TERM TREATMENT WITH ELAFIBRANOR LEADS TO BIOCHEMICAL AND SYMPTOMATIC IMPROVEMENTS FOR AT LEAST 3 YEARS IN PATIENTS WITH PRIMARY BILIARY CHOLANGITIS.AASLD 2025,LBA-5016.
2. Christopher Bowlus,Gideon Hirschfield,Alejandra Villami,et al.DISEASE CONTROL AS EVIDENCED BY LONGITUDINAL TRANSIENT ELASTOGRAPHY MEASUREMENTS IN THE ASSURE STUDY: 36 MONTHS OF TREATMENT WITH SELADELPAR IS ASSOCIATED WITH STABLE OR IMPROVED LIVER STIFFNESS IN PATIENTS WITH PRIMARY BILIARY CHOLANGITIS.AASLD 2025,LBA-5031.
3. Molly Frey,Christopher Bowlus,Adam Elhofy,et al.CNP-104 DEMONSTRATES CLINICAL BENEFITS IN PRIMARY BILIARY CHOLANGITIS (PBC) THROUGH IMPROVED COMPOSITE BIOCHEMICAL MARKERS AND PROGNOSTIC SCORES.AASLD 2025,Abstract-4399.
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)