
胆囊癌是胆道系统最常见且死亡率极高的恶性肿瘤,其全球发病率不断上升,具有隐匿性、发展速度快、预后差等恶性肿瘤的典型特征。早期胆囊癌症状并不显著,发现时多已为晚期,常伴随浸润转移,且手术切除率低,仅25%的患者具备手术机会,5年生存率不足10%。
2010年发表在新英格兰杂志上的ABC-02试验确定了吉西他滨联合顺铂(GC)作为包括胆囊癌在内的晚期胆管恶性肿瘤一线标准化疗方案,但是应用该疗法的中位无进展生存期(PFS)和总生存期(OS)仅为8.0和11.7个月。随着近年来免疫检查点抑制剂的不断发展,为肿瘤治疗带来了新机遇。程序性细胞死亡蛋白-1(PD-1)作为一种抑制性免疫分子,与其配体细胞程序性死亡-配体1(PD-L1)结合后可引发免疫抑制反应,使肿瘤细胞能够逃避免疫系统的攻击,而PD-1抑制剂可通过阻断PD-1/PD-L1通路,恢复免疫系统对肿瘤细胞的攻击。TOPAZ-1和KEYNOTE-966两项Ⅲ期试验已表明GC方案联合免疫抑制剂的疗效及安全性,现已作为晚期胆囊癌患者的新一线治疗方案。
甲磺酸阿帕替尼是一种血管内皮生长因子(VEGF)通路抑制剂,通过抑制VEGFR-2信号传导途径来减少肿瘤的血液供应和新生血管的形成,现已在非小细胞肺癌、恶性黑色素瘤、胃癌及肝癌等多种肿瘤中发挥作用。目前在晚期胆囊癌的临床研究中也显示出其较好的预后及安全性,为晚期胆囊癌患者提供了新的治疗选择。
随着靶向治疗和免疫疗法的不断发展,肿瘤治疗正逐步进入个体化精准医疗时代,与传统的化学疗法联合应用往往能表现出显著的临床效果。本研究通过探讨甲磺酸阿帕替尼联合GC+卡瑞丽珠单抗治疗晚期胆囊癌的效果及安全性,为临床治疗提供新的证据。

1资料与方法
本研究为多中心回顾性分析,选取2022年1月—2023年12月郑州大学人民医院及郑州大学附属肿瘤医院收治的晚期胆囊癌患者,并根据纳入和排除标准进行筛选。鉴于郑州大学附属肿瘤医院该类病例数量较少,为确保数据分析的统计效能,本研究将其统一分析,未予以单独分组。所有病例均由两名经验丰富的高年资主治医师严格审核,从两个医院收集的病例筛选标准经过严格制定并保持统一,以确保数据准确性和研究可靠性。纳入标准:(1)经病理学确认的胆囊癌,临床总TNM分期均为Ⅳ期(肿瘤均已侵袭、转移至肝脏或其他脏器);(2)CT或MRI检查发现至少存在1个可测量病灶;(3)肝功能Child-Pugh分级为A~B级;(4)年龄18~80岁;(5)具备完整的临床资料和随访资料。排除标准:(1)合并其他恶性肿瘤;(2)曾使用其他抗肿瘤治疗(如化疗、放疗、其他靶向药物及免疫抑制剂等);(3)存在严重心、肾功能不全,合并凝血功能障碍;(4)缺乏充足的随访资料;(5)临床总TNM分期为Ⅰ~Ⅲ期。最后共筛选出75例入组病例。
将入组病例分为研究组和对照组。研究组(甲磺酸阿帕替尼联合GC+卡瑞丽珠单抗治疗方案):甲磺酸阿帕替尼片口服(250 mg/次,1次/d,餐后半小时后以温水送服),若无法耐受适当减量;吉西他滨静脉输注(1 000 mg/m2,第1天及第8天应用);顺铂静脉输注(25 mg/m2,第1天及第8天应用);卡瑞丽珠单抗(艾瑞卡®)静脉滴注(200 mg/次,若体质量2,第1天及第8天应用);顺铂静脉输注(25 mg/m2,第1天及第8天应用);卡瑞丽珠单抗(艾瑞卡®)静脉滴注(200 mg/次,若体质量
(1)参照根据mRECIST(改良实体瘤疗效评价标准)对两组患者的近期疗效进行评价。完全缓解(CR):所有靶病灶完全消失;部分缓解(PR):所有可测量靶病灶的直径总和较基线减少至少30%;疾病稳定(SD):靶病灶的缩小程度未达到PR标准,且增大幅度未达到PD标准;疾病进展(PD):所有测量的靶病灶直径总和较基线增加至少20%,且绝对增长值≥5 mm,或出现新的病灶;客观缓解率(ORR):ORR=CR+PR的患者比例,反映肿瘤显著缩小的比例;疾病控制率(DCR):DCR=CR+PR+SD的患者比例,评估治疗对疾病控制的有效性。(2)通过回顾性分析患者住院期间的各项检验指标及病史记录,按照常见不良事件评价标准(CTCAE 5.0版)对各种不良反应评级并记录。(3)随访方式:电话或门诊随访,末次随访时间至2024年12月,并记录患者PFS及OS。

2结果
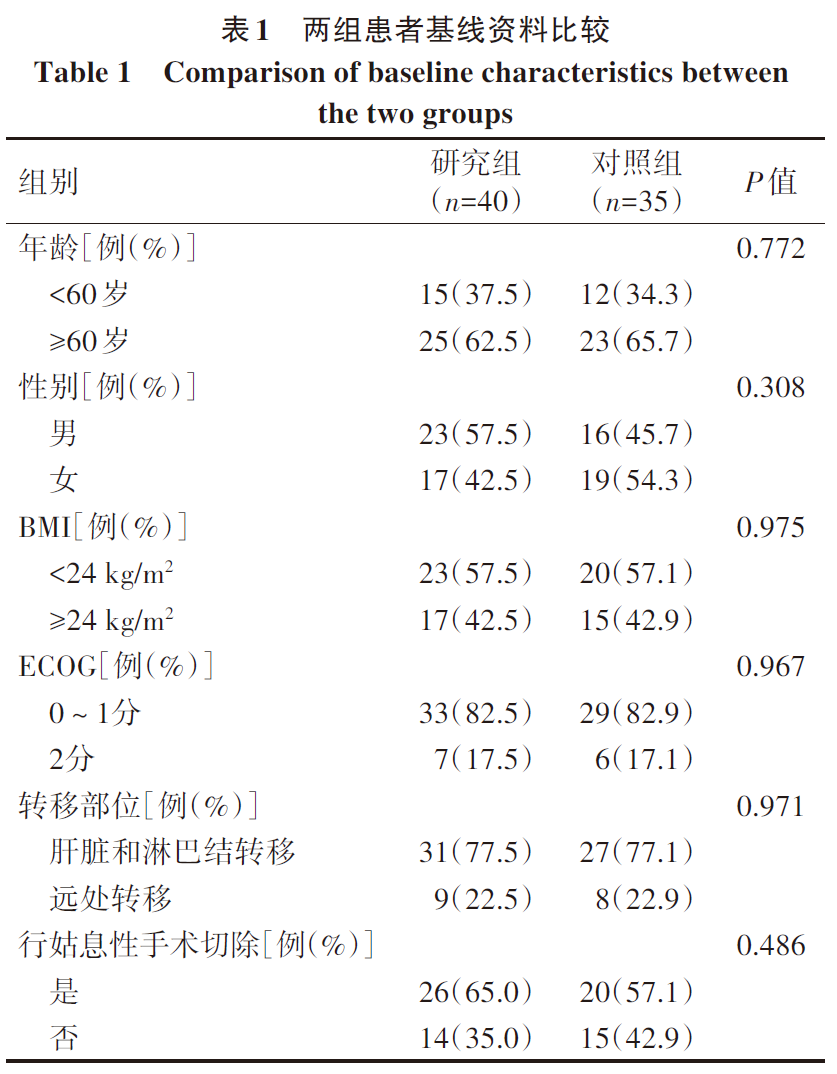
将两组患者的临床基线资料进行比较,差异均无统计学意义(P值均>0.05),具有可比性(表1)。
两组ORR分别为35.0%、17.1%,差异无统计学意义(χ²=3.044,P>0.05);两组DCR分别为80.0%、65.7%,差异无统计学意义(χ²=1.948,P>0.05)(表2)。随访期间未出现失访病例。研究组22例死亡,1年生存率达45.0%;对照组28例死亡,1年生存率达20.0%,差异具有统计学意义(χ²=5.25,PCI:4.39~11.01),对照组为4.17个月(95%CI:3.48~4.85),差异有统计学意义(χ²=16.735,PCI:8.07~15.47),对照组为7.97个月(95%CI:5.84~10.09),差异无统计学意义(χ²=2.311,P>0.05)(图1、2)。
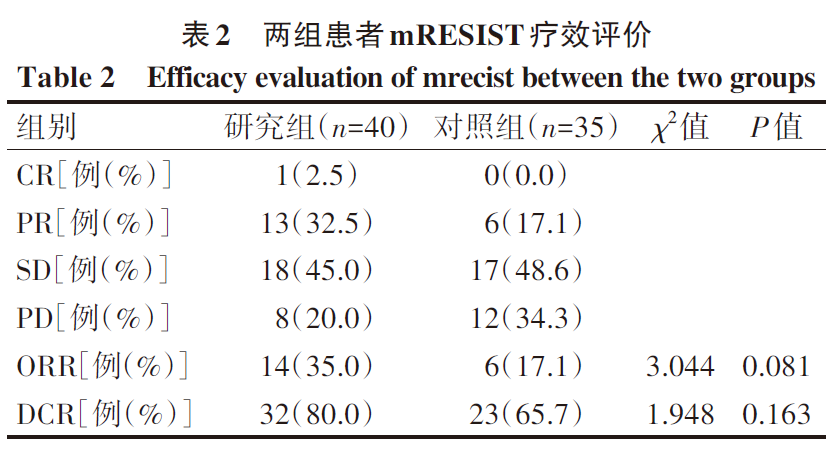

图1 两组间PFS对比的生存曲线
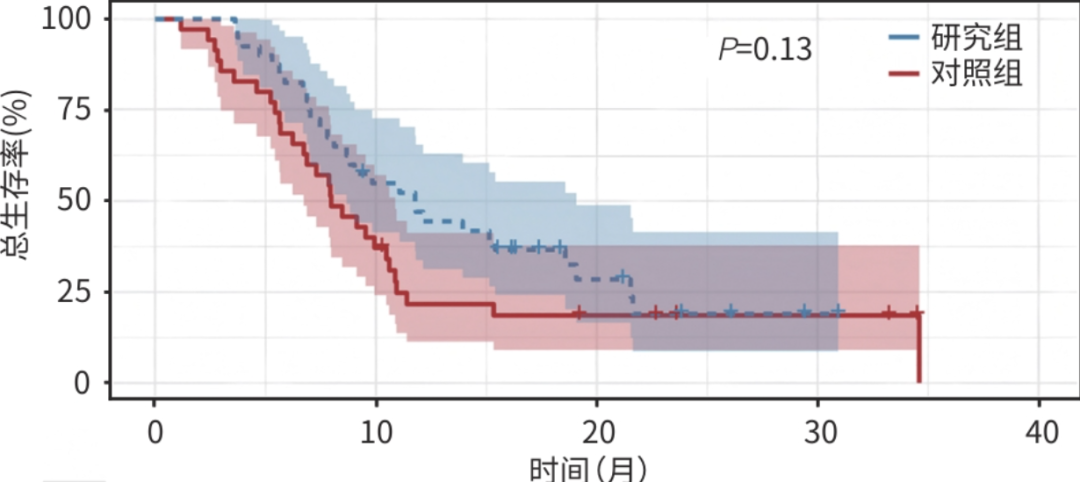
图2 两组间OS对比的生存曲线
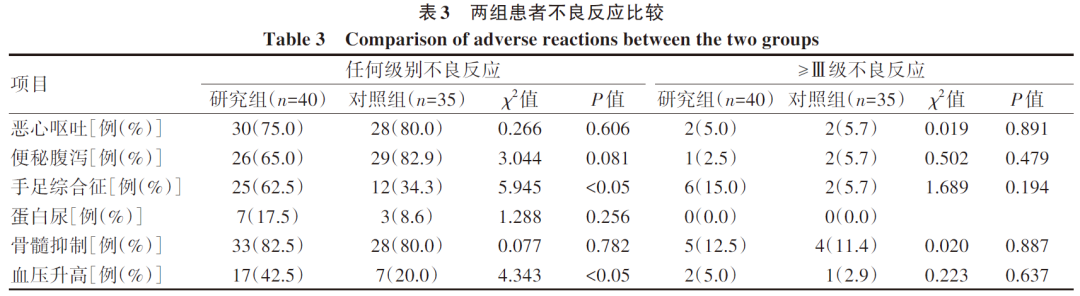
两组患者均存在不同程度的不良反应。研究组患者任何级别的不良反应中手足综合征和血压升高的发生率高于对照组,差异均具有统计学意义(P值均P值均>0.05)(表3)。

3讨论
胆囊癌是一种具有高异质性、强侵袭性的恶性肿瘤,大部分患者在初诊时已处于晚期,失去了手术根治切除的机会,通常只能接受药物系统治疗。自ABC-02研究公布以来的十余年间,GC方案对晚期胆囊癌患者的生存改善有限,已难以满足现阶段的临床需求。因此,寻找新的治疗策略迫在眉睫。随着TOPAZ-1与KEYNOTE-966这两项研究结果的公布,度伐利尤单抗联合GC及帕博利珠单抗联合GC分别在2022年和2023年《CSCO胆道恶性肿瘤诊疗指南》中获Ⅰ级推荐(证据级别1A)。而随着靶向免疫治疗的发展,“三联四药”方案受到了越来越多的关注。通过在靶向联合免疫治疗的基础上加入化疗,增强抗肿瘤免疫反应并在多个层面对肿瘤进行攻击,从而实现互补与协同作用。
2022年ESMO年会上报道的替雷利珠单抗+仑伐替尼+GEMOX方案治疗潜在可切除的局部晚期胆管癌的临床研究结果显示,ORR为56%,DCR为92%,转化治疗后R0切除率高达52%。2023年一项Ⅱ期研究评估Gemox联合PD-1单抗和仑伐替尼治疗不可切除肝内胆管癌的疗效,结果显示ORR达80%,DCR达93.3%,中位OS、PFS和缓解持续时间分别为22.5、10.2和11.0个月。2023年一项仑伐替尼和PD-1/PD-L1抑制剂联合Gemox化疗治疗晚期胆道癌患者的研究结果显示,ORR为64%,DCR为96%,中位OS、PFS分别为25.0和12.13个月。“三联四药”方案在晚期胆道癌的治疗中展现出显著效果和可控的安全性,为晚期胆囊癌的治疗提供了新的思路。因此,甲磺酸阿帕替尼联合GC+卡瑞丽珠单抗方案治疗晚期胆囊癌具有良好的理论依据和可行性。
本研究样本源于两个大型临床研究中心,数据真实可靠。结果显示,研究组患者的ORR和DCR差异无统计学意义。随访结果表明,研究组的1年病死率显著低于对照组,中位PFS明显延长,差异具有统计学意义;中位OS差异无统计学意义。因此,本研究提示,甲磺酸阿帕替尼联合GC+卡瑞丽珠单抗在延长晚期胆囊癌患者PFS方面表现更为显著,具有潜在的临床决策指导价值。
药物的不良反应是临床治疗中需要重点关注的方面。本治疗方案联用药物较多,为此本文仔细回顾并研究了所有入组患者的检验结果及病史资料,对其发生的不良反应做了严谨、客观的分级评价。研究组患者任何级别的不良反应中手足综合征和血压升高的发生率高于对照组,差异均具有统计学意义(P值均
另外,本研究在收集病例资料时发现1例胆囊癌肝内转移患者(属于本次研究排除标准内患者),原定治疗方案为GC+卡瑞丽珠单抗,用药3个月后复查提示肿瘤未进展,后因患者个人要求,遂更改治疗方案为甲磺酸阿帕替尼联合GC+卡瑞丽珠单抗。应用此方案后每2个月复查影像学提示肝转移瘤体缩小20%,用药8个月后瘤体体积缩小50%,已达到PR标准,后因自身原因停药2个月,再次复查发现肿瘤已转移至肺脏及腹腔。虽未纳入本次研究,但也反映出甲磺酸阿帕替尼联合GC+卡瑞丽珠单抗方案的疗效。
综上,甲磺酸阿帕替尼联合GC+卡瑞丽珠单抗方案为晚期胆囊癌患者提供了一种有效且安全的选择,可取得较好的近期疗效。但本研究也存在一定的局限性,如为回顾性研究、样本量较小、随访时间较短。因此,有必要扩大样本量、延长随访时间,通过前瞻性研究进一步验证该方案对晚期胆囊癌患者的疗效和安全性。随着研究的深入,化疗联合靶向免疫治疗在未来有望成为晚期胆囊癌的标准治疗,改善患者预后。

https://www.lcgdbzz.org/cn/article/doi/10.12449/JCH250726

来源:临床肝胆病杂志
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)