
进行性肺纤维化(PPF)是一类以肺纤维化进行性恶化为核心特征的间质性肺疾病(ILD)亚型,可由多种病因引发,与特发性肺纤维化(IPF)共享关键病理机制,却又因病因多样性呈现更复杂的临床图景。当前治疗虽能延缓进展,但无法逆转纤维化,探索新疗法已成为临床迫切需求。本文将系统梳理PPF的诊疗现状与最新进展,解析前沿治疗靶点及未来方向。
PPF并非独立疾病,而是一组具有共同进展特征的ILD亚型。2022年美国胸科学会/欧洲呼吸学会等联合指南将其定义为:非IPF的ILD患者,在过去1年内出现呼吸道症状恶化(无其他解释)、肺功能或影像学进展证据中的至少两项。这一定义凸显了其与IPF的“同源性”——两者均以不可逆的肺纤维化进展和肺功能下降为核心,但PPF病因更广,涵盖结缔组织病相关ILD、结节病等多种基础疾病。
从临床数据看,PPF的预后虽略优于IPF,但仍不容乐观。IPF的全球患病率约为4/10000,确诊后中位生存期仅5-7年;而PPF患者虽因基础病差异生存期波动较大,但肺功能年下降率与IPF相近,且急性加重风险同样显著,严重影响生活质量。
目前,PPF的治疗以抗纤维化药物为核心,尼达尼布和吡非尼酮是两大支柱,但两者的适用场景与证据强度存在差异。
尼达尼布:跨亚型的广谱作用
尼达尼布是一种多靶点酪氨酸激酶抑制剂,通过抑制血管内皮生长因子受体(VEGFR)、血小板衍生生长因子受体(PDGFR)等,阻断成纤维细胞增殖与胞外基质(ECM)分泌。在INBUILD试验中,尼达尼布使PPF患者1年内用力肺活量(FVC)下降速率较安慰剂减缓57%,且疗效不受基础ILD亚型或影像学模式影响,这一结果推动其成为首个获FDA和EMA批准用于PPF的药物。
后续真实世界研究进一步验证了其价值:一项多中心观察性研究显示,尼达尼布可降低PPF患者的疾病进展风险,且在系统性硬化症相关ILD(SSc-ILD)等特定亚型中,虽疗效稍弱但仍显著优于安慰剂。
吡非尼酮:潜力待挖掘的抗纤维化药
吡非尼酮通过抑制转化生长因子-β(TGF-β)、肿瘤坏死因子等炎症因子发挥作用,目前主要获批用于IPF,但在PPF中的探索已取得积极信号。RELIEF试验虽因招募缓慢提前终止,但数据显示吡非尼酮可减少PPF患者的FVC下降;另一项针对未分类ILD的Ⅱ期试验也证实,其能延缓肺功能恶化,尤其对影像学呈现普通型间质性肺炎(UIP)模式的患者更有效。
值得关注的是,吸入性吡非尼酮的研发改善了口服制剂的胃肠道不良反应,其Ⅱ期试验显示良好安全性,目前全球多中心Ⅲ期试验正评估其联合标准治疗的疗效。此外,吡非尼酮与尼达尼布的联合疗法也在探索中,法国一项Ⅳ期试验对比“联合治疗”与“单药切换”对难治性IPF的效果,结果或将为PPF的联合治疗提供参考。
PPF与IPF共享TGF-β激活、成纤维细胞异常活化等关键通路,为新疗法提供了多个潜在靶点。近年来,多项Ⅱ/Ⅲ期试验已证实一批候选药物的潜力,涵盖整合素抑制、磷酸二酯酶调控等多个方向。
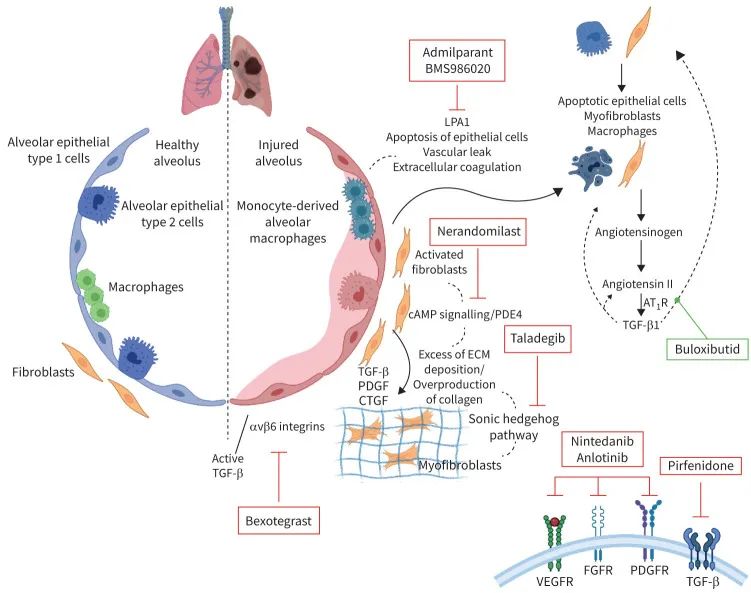
图1 参与纤维化发病机制的特定分子途径和新的治疗靶点
整合素抑制剂:TGF-β激活的“开关”
TGF-β是纤维化的核心驱动因子,其活性依赖于αvβ6和αvβ1整合素的激活。Bexotegrast(PLN-74809)作为口服双靶点整合素抑制剂,在小鼠模型中展现出比临床剂量的尼达尼布和吡非尼酮更强的抗胶原沉积作用。Ⅰ期临床试验(INTEGRIS-IPF)显示,其在119例IPF患者中安全性良好,治疗组与安慰剂组的不良事件发生率相近(69.7% vs 67.7%),且探索性终点显示FVC下降减缓、肺纤维化程度减轻。目前,Ⅲ期试验BEACON-IPF正进一步验证其疗效,有望成为首个靶向整合素的PPF治疗药物。
PDE4抑制剂:双重调控炎症与纤维化
磷酸二酯酶4(PDE4)通过降解环磷酸腺苷(cAMP)削弱抗纤维化介质(如前列腺素E2)的作用。Nerandomilast作为选择性PDE4B抑制剂,在Ⅱ期试验中使IPF患者12周内FVC下降速率较安慰剂减少42%,且与尼达尼布联用具有协同效应。其Ⅲ期试验FIBRONEER-IPF已达到主要终点(52周FVC变化),有望近期提交上市申请。
针对PPF的FIBRONEER-ILD试验也达到了主要终点,研究显示,第52周时,与安慰剂组相比,nerandomilast两种剂量组均显著减少了FVC的下降。Nerandomilast9mg组FVC绝对值的下降相比安慰剂组减少了81.1mL(95%Cl:46.0,116.3;P<0.001),nerandomilast 18mg组FVC绝对值的下降相比安慰剂组减少了67.2mL(95% C:31.9,102.5;P<0.001)。亚组分析显示,无论是否接受尼达尼布背景治疗,治疗第52周时,与安慰剂组相比nerandomilast均可减少FVC绝对值下降。
在次要终点方面,截至第一次数据库锁定时,nerandomilast 18mg组发生首次急性加重或死亡、因呼吸系统原因住院或死亡、以及死亡的风险相比安慰剂组存在名义上的显著降低:首次急性加重或死亡的风险(HR=0.59,95% CI:0.41,0.84);因呼吸系统原因住院或死亡的风险(HR=0.75,95% CI:0.56,1.00);死亡风险(HR=0.48,95% CI:0.30,0.79)。
溶血磷脂酸拮抗剂:阻断纤维化“信号传递”
溶血磷脂酸(LPA)通过LPA1受体促进上皮细胞凋亡、成纤维细胞募集,在IPF患者的肺泡灌洗液中水平显著升高。Admilparant(BMS-986278)作为LPA1拮抗剂,在Ⅱ期试验中使IPF/PPF患者26周FVC下降较安慰剂减少56%,且无论是否联用基础抗纤维化药均有效。目前,两项针对IPF和PPF的Ⅲ期试验正验证其长期疗效,而另一种自分泌运动因子抑制剂BBT-877也进入Ⅱ期研发,为该通路提供更多治疗选择。
吸入性曲前列尼尔:局部靶向抗纤维化
曲前列尼尔是前列环素受体激动剂,通过激活G蛋白偶联通路升高蛋白激酶A水平,抑制成纤维细胞增殖与胶原合成。吸入制剂可直接作用于肺部,减少全身不良反应。在INCREASE试验中,它使ILD相关肺动脉高压患者6分钟步行距离显著增加,事后分析显示IPF亚组FVC改善达168.5mL。目前,针对IPF的TETONⅠ/Ⅱ试验和针对PPF的TETON-PPF试验正评估其52周FVC变化,长期扩展性试验TETON-OLE则聚焦安全性,有望为PPF合并血管病变患者提供新选择。
其他潜力药物
hedgehog抑制剂:Taladegib(ENV-101)通过抑制Smoothened蛋白阻断 hedgehog通路,在Ⅱa试验中使IPF患者FVC显著改善,但需关注脱发、肌痉挛等不良反应。Ⅱb试验WHISTLE-PF将探索其在IPF/PPF中的剂量优化方案。
酪氨酸激酶抑制剂:安罗替尼(已获批用于肺癌)通过抑制TGF-β1信号通路减轻小鼠肺纤维化,中国Ⅲ期试验正评估其对IPF/PPF患者FVC的影响。
血管紧张素Ⅱ型受体激动剂:Buloxibutid(C21)激活AT2R发挥抗纤维化作用,Ⅱ期AIR试验显示IPF患者耐受良好,52周全球Ⅲ期试验ASPIRE结果值得期待。
PPF常继发于系统性硬化症、类风湿关节炎等疾病,这些基础病的治疗进展也为PPF管理提供参考。
系统性硬化症相关ILD(SSc-ILD)
指南推荐吗替麦考酚酯为一线用药,尼达尼布为进展期首选。新型药物中,Belimumab(靶向B淋巴细胞刺激因子)的Ⅲ期试验(BLISSc-ILD)正探索其对B细胞异常活化的调控作用;Efzofitimod(靶向 neuropilin-2)通过减少炎症因子改善纤维化,Ⅱ期试验显示可降低激素依赖,目前已启动SSc-ILD适应症研究。
类风湿关节炎相关ILD(RA-ILD)
尼达尼布在结缔组织病相关ILD中的数据支持其用于RA-ILD,但吡非尼酮相关试验因提前终止结果有限。Abatacept(CTLA4-Ig)的Ⅱ期试验正评估其安全性,有望为免疫介导的纤维化提供新方向。
结节病相关纤维化
约5%的结节病患者进展为肺纤维化,NINSARC试验探索尼达尼布的疗效,而Efzofitimod在Ⅱb试验中显示可减少肉芽肿复发,XTMAB-16(靶向TL1A)则聚焦肉芽肿形成机制,为这类患者提供新希望。
PPF诊疗正迈向“精准化”与“多维度”,但仍面临多重挑战。
新兴治疗方向
细胞与外泌体治疗:间充质干细胞通过免疫调节、促进上皮修复发挥潜力,早期试验(NCT02594839)显示对PPF安全;外泌体携带的miRNA可调控成纤维细胞活性,有望成为“无细胞治疗”新载体。
组学与基因治疗:整合转录组学与蛋白质组学可识别PPF分子亚型,指导个性化治疗;CRISPR技术靶向纠正MUC5B等基因突变,虽处于早期,但为根治纤维化提供可能。
联合治疗:针对TGF-β、LPA等多通路的联合方案(如尼达尼布+PDE4抑制剂)可能突破单药局限,目前多项Ⅱ期试验正在探索最优组合。
核心挑战
疾病异质性:PPF病因复杂,需通过生物标志物(如血液SP-D、MMP-7)实现患者分层,避免“一刀切”治疗。
临床试验设计:需优化终点指标(如结合影像学定量分析),解决招募困难问题,推动真实世界数据与随机试验的结合。
安全性平衡:新药物如 hedgehog抑制剂的不良反应需通过剂量调整或联合干预减轻,确保获益风险比。
PPF的治疗已从“单一抗纤维化”进入“多靶点协同”时代,尼达尼布与吡非尼酮奠定了基础,而整合素抑制剂、PDE4抑制剂等新药的涌现,有望突破“只能延缓、无法逆转”的瓶颈。未来,随着组学技术、基因编辑等工具的应用,PPF诊疗将逐步实现从“对症治疗”到“病因根治”的跨越,为患者带来更多生存希望。但与此同时,如何平衡疗效与安全性、实现个体化治疗,仍是需要持续探索的核心课题。

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)