医脉通编辑整理,未经授权请勿转载。
Evorpacept(ALX148)是一种新型的工程融合蛋白。ASPEN-01 研究的初步结果显示,单药 Evorpacept 具有良好的安全性,未达到最大耐受剂量(MTD)(最大给药剂量:每周一次 10 mg/kg;每两周一次 30 mg/kg),并且与
ASPEN-01研究于2017年3月至2022年2月在美国和韩国的10个中心开展。3患者接受静脉注射Evorpacept(10 mg/kg或15 mg/kg,每周一次,持续至疾病进展)联合固定疗程的静脉注射利妥昔单抗(375 mg/m²,前4周每周一次,后续每4周一次,持续8个月)。
患者年龄≥18岁,患有惰性或侵袭性复发/难治性CD20阳性B细胞 NHL,既往接受过≥1线抗肿瘤治疗,根据2014年Lugano标准至少有一个可测量病灶,骨髓、肾脏和肝脏功能良好,且东部肿瘤协作组(ECOG)体能状态评分为0或1。
主要终点是确定Evorpacept与利妥昔单抗联合使用时的最大耐受剂量(MTD)。次要终点包括安全性、药代动力学(PK)、免疫原性、最佳客观肿瘤反应(使用Lugano标准)、客观缓解率(ORR)、缓解持续时间、无进展生存期和总生存期。
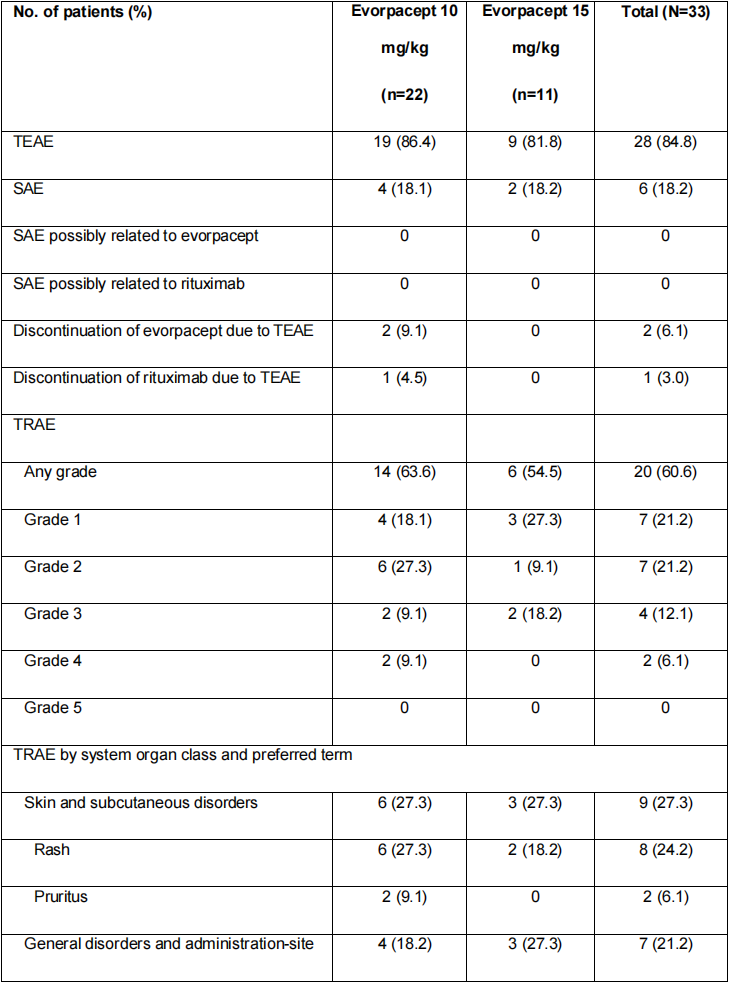
共33例R/R NHL患者纳入研究(表1),接受了至少1剂研究药物治疗。22例(66.7%)患者服用10 mg/kg Evorpacept,11例(33.3%)患者服用15 mg/kg Evorpacept。Evorpacept和利妥昔单抗的中位治疗持续时间分别为16周(范围,0-118周)和15周(范围,0-39周)。1例患者在数据截止日期仍在接受治疗。
表1


结果显示联合治疗方案耐受性良好,未出现剂量限制性毒性或未发现最大耐受剂量,最常见治疗相关不良事件为
表2
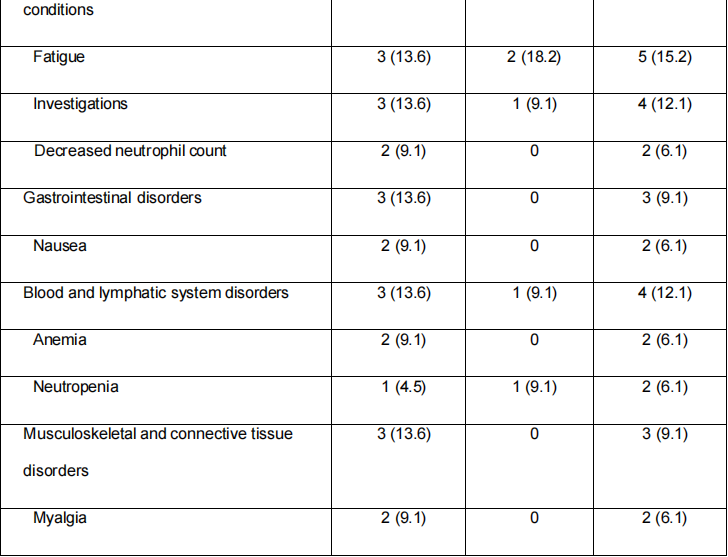
药代动力学/药效学特征与既往研究一致,两种剂量组均实现CD47靶点完全占据(85%)。在可评估疗效患者(n=32)中,客观缓解率(ORR)为50.0%(95%置信区间:33.1%–69.8%;表3)。
表3
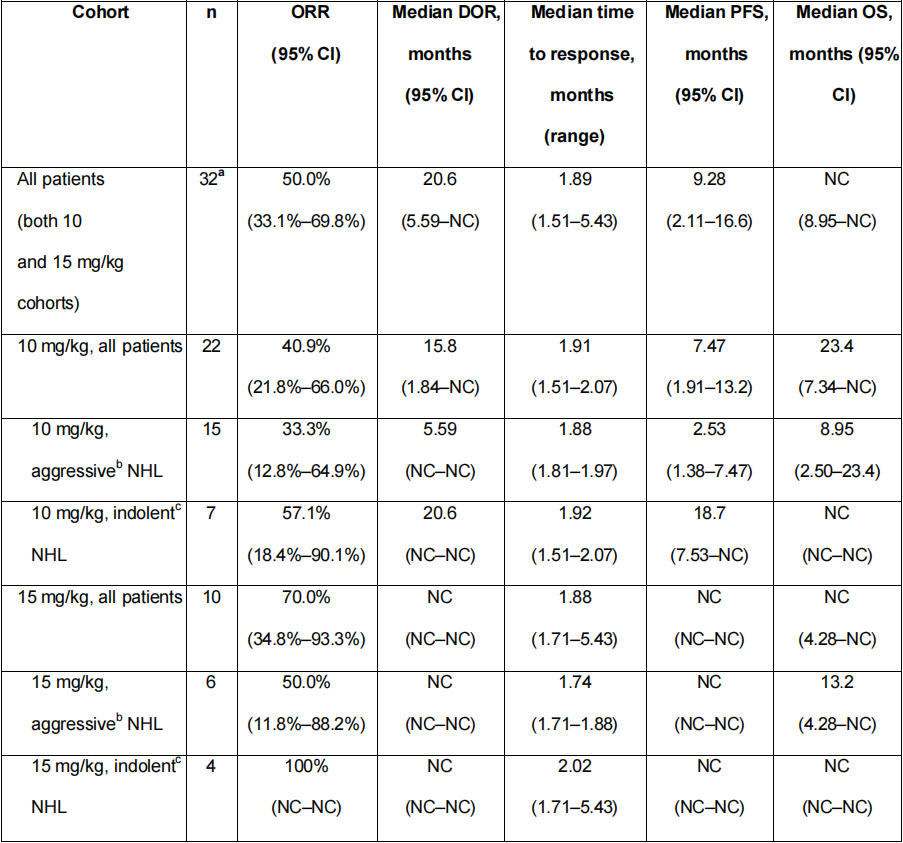
总之,来自首次在人体中进行的I期ASPEN-01研究的分析表明,Evorpacept与利妥昔单抗联合使用在复发/难治性(R/R)
本研究首次报道的Evorpacept(一种通过灭活Fc结构域优化安全性的CD47-SIRPα靶向融合蛋白)联合利妥昔单抗治疗复发/难治性B-NHL的I期数据具有重要临床意义:从机制上看,CD47阻断可解除肿瘤细胞的“别吃我”信号,而Evorpacept的Fc改造使其血液学毒性(仅1例3级贫血)显著低于传统抗CD47抗体,这为后续联合治疗提供了更安全的平台;疗效方面,50%的客观缓解率在重度经治患者中显示出潜力,提示CD47抑制可能增强利妥昔单抗的抗体依赖性细胞吞噬(ADCP)效应,但需注意该研究未报告完全缓解率且样本量较小,需在II期扩展队列中验证疗效深度。安全性方面,3-4级中性粒细胞减少发生率(12.1%)低于化疗方案,但皮疹(24.2%)等非血液毒性提示需关注免疫激活相关不良事件。未来需探索生物标志物(如肿瘤CD47表达水平、巨噬细胞浸润程度)以精准筛选获益人群,并设计联合双特异性抗体或ADC药物的增效方案。综上,该研究为CD47靶向治疗的临床转化提供了关键循证依据,但其治疗地位需通过随机对照试验进一步确立。

主任医师,教授,博士研究生导师,博士后合作导师
教育部“中国科技论文在线”特邀评审专家
教育部新世纪优秀人才
欧洲肿瘤内科协会抗癌分会会员
中国免疫学学会会员
中美医学科学与工程协会会员
广东省医疗行业协会
广东省医师协会血液科医师分会副主任委员
广东省医疗安全协会血液学分会副主任委员
广东省健康管理学会血液病分会副主任委员
广州抗癌协会理事会常务理事
广东省医学会血液病学分会常员
广东省抗癌协会血液学分会常委
从事血液病学医教研工作30余年,目前担任教育部硕博士论文的评审专家,自2006年担任欧洲SCI杂志AntiCancer Drugs 常务编委,Ann Hematol 编委。目前已主持国家自然科学基金5项,省部级科研基金10余项,在国内外核心期刊发表论文200余篇,其中在Ann Oncol(IF>50)、American J Hematol. Blood 等杂志发表SCI收录论文50余篇。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)