中重度斑块状银屑病的系统治疗仍存在未被满足的临床需求:现有口服小分子药物或生物制剂在疗效或耐受性方面各有局限。SYHX1901是一种新型口服化合物,可同时抑制JAK1‑3和脾酪氨酸激酶(SYK),从而阻断IL‑23/IL‑17轴及B细胞依赖的炎症放大环路。近日,一项由复旦大学附属华山医院
研究设计
本研究为一项多中心、随机、双盲、安慰剂对照的II期临床试验,在中国15个中心开展。纳入标准:18-75岁成人,稳定中重度斑块状银屑病(PASI ≥12,静态医师总体评估[sPGA] ≥3,体表面积[BSA] ≥10%)至少6个月。患者按1:1:1:1随机分配至口服SYHX1901 60mg、90mg、180mg或安慰剂组,每日一次,治疗12周。随机化分层因素为既往是否使用过生物制剂。
评估指标
-主要终点:第12周时达到PASI 75(银屑病面积与严重程度指数较基线改善≥75%)的患者比例。
-次要终点:PASI 50、PASI 90、sPGA 0/1(清除/几乎清除)、皮肤病生活质量指数(DLQI)0/1应答率,以及BSA较基线的百分比变化。
-安全性:不良事件(AE)、治疗期间出现的不良事件(TEAE)、实验室检查等。
统计分析
采用逻辑回归模型,校正分组、既往生物制剂使用史、基线PASI、基线BMI及是否合并
患者基线特征
共筛选135例患者,93例接受至少一剂研究药物(60mg组23例、90mg组23例、180mg组24例、安慰剂组23例)。77%为男性,平均年龄45.4岁。各组基线特征均衡。
疗效结果
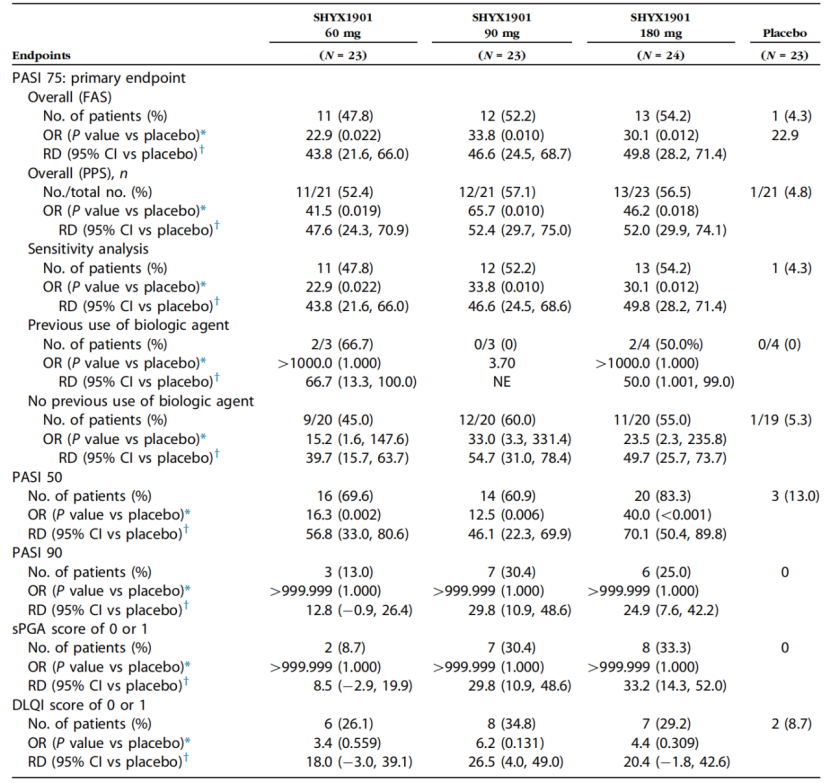
主要终点(PASI 75):第12周时,SYHX1901 60mg、90mg、180mg组的PASI 75应答率分别为47.8%(11/23)、52.2%(12/23) 和54.2%(13/24),均显著高于安慰剂组的4.3%(1/23)(P值分别为0.022、0.010、0.012)。符合方案集分析结果一致(表I,原文第2页 Table I)。
次要终点:
-PASI 50:各剂量组分别为69.6%、60.9%、83.3%,安慰剂组13.0%(均P<0.01)。
-PASI 90:13.0%、30.4%、25.0% vs 0%。
-sPGA 0/1:8.7%、30.4%、33.3% vs 0%。
-DLQI 0/1:26.1%、34.8%、29.2% vs 8.7%。
-BSA较基线变化:分别下降48.3%、45.3%、52.8%,安慰剂组变化不显著(均P<0.001)。
起效时间:治疗第2周即观察到PASI 75应答,并持续至第12周。
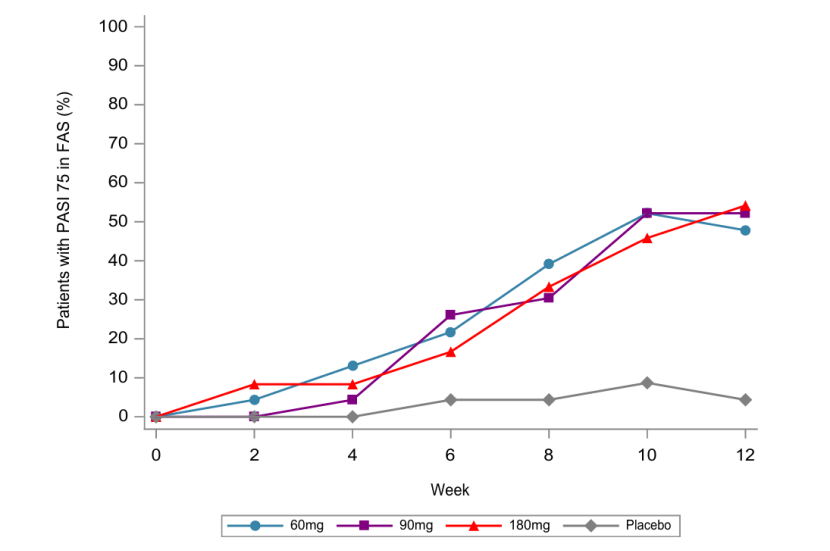
图1 第 0-12 周各治疗组 PASI 75 应答率变化
既往生物制剂使用史亚组:在既往使用过生物制剂的少数患者中(60mg组3例、180mg组4例),SYHX1901仍显示出较高应答率(60mg组66.7%,180mg组50.0%);未使用过生物制剂的患者中,各剂量组PASI 75应答率为45.0%~60.0%(表I)。
表1:第12周疗效结果汇总(PASI 75/50/90、sPGA 0/1、DLQI 0/1应答率及BSA变化)
安全性结果
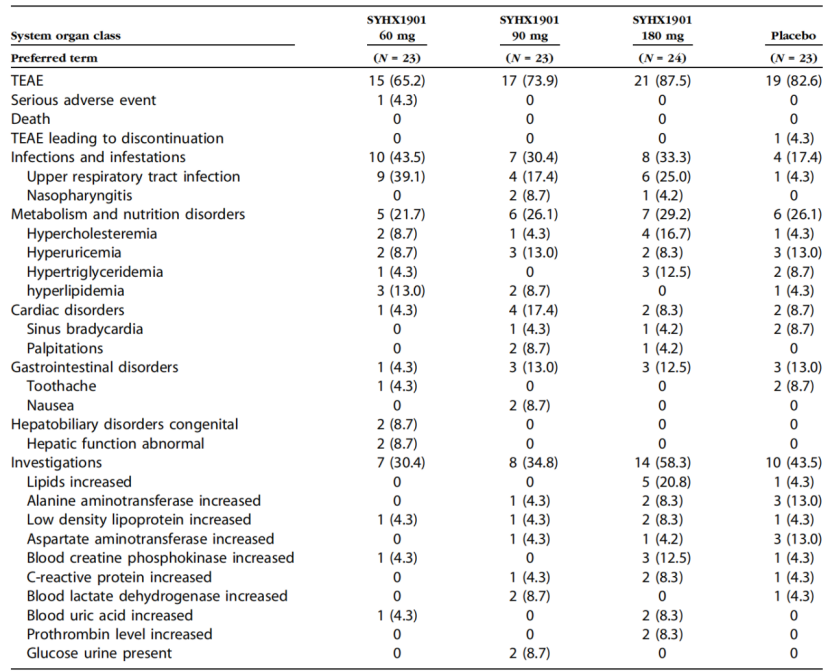
总体TEAE:治疗期间出现的不良事件发生率在60mg、90mg、180mg及安慰剂组分别为65.2%、73.9%、87.5%和82.6%。多数为轻中度。
最常见不良事件:
表2 各治疗组中发生率≥5% 的治疗期间不良事件(SS)
-
-鼻
-
-肝酶升高:ALT升高(0%~8.3%)、AST升高(0%~4.2%)。
-肌酸激酶升高:180mg组12.5%。
严重不良事件及停药:仅60mg组1例患者发生严重不良事件(头晕和胸部不适)。无死亡。仅安慰剂组1例因TEAE停药。未观察到JAK抑制剂相关的黑框警告事件(严重感染、死亡、恶性肿瘤、主要心血管不良事件、血栓)。
本研究首次报道了口服双JAK/SYK抑制剂SYHX1901治疗中重度斑块状银屑病的II期临床数据。主要发现如下:
1.疗效明确:治疗12周时,SYHX1901 60~180mg每日一次可使约半数患者达到PASI 75,且呈现剂量依赖性趋势(180mg组PASI 75应答率54.2%)。PASI 90和sPGA 0/1应答率在90mg和180mg组达到25%~33%。
2.起效迅速:治疗第2周即观察到应答,提示该药可能快速控制炎症。
3.感染风险可控:上呼吸道感染发生率增加(39% vs 安慰剂4.3%),与JAK抑制剂和TYK2抑制剂的已知风险一致,但均为轻中度,无严重机会性感染。
4.血脂和肝酶影响:SYHX1901组出现一定比例的血脂升高和肝酶升高,但未导致停药,需长期随访评估。
5.无黑框警告事件:在12周治疗期内,未观察到血栓、主要心血管不良事件或恶性肿瘤,与选择性JAK1抑制剂或TYK2抑制剂的安全性特征相似。SYHX1901在中重度斑块状银屑病患者中显示出快速、剂量依赖的
参考文献
医脉通是专业的在线医生平台,“感知世界医学