前言:2026年4月22日,新一代靶向TROP2抗体偶联药物(ADC)德达博妥单抗(Dato-DXd)在中国正式商业上市,首批药品将陆续在全国各地医院及药房投入临床使用。这一进展为众多内分泌且一线化疗经治的HR+/HER2-晚期
“疗效+安全性”双优,
Dato-DXd为HR+/HER2-晚期乳腺癌治疗提供新选择
HR+/HER2-是乳腺癌中最常见的分子亚型,约占所有乳腺癌的70%[1]。当前,内分泌治疗联合CDK4/6抑制剂是这类患者的标准一线治疗方案。然而,对于内分泌治疗进展后出现耐药,尤其是HER2 IHC 0的患者,后续治疗选择尚无统一标准,始终是临床实践的难点。传统化疗虽为常用方案,但其疗效有限且伴随明显的毒副反应,严重影响患者生活质量,临床对高效、低毒的精准治疗的需求极为迫切[2]。
针对这一临床困境,全球III期随机对照研究——TB01应运而生,研究聚焦内分泌治疗耐药且化疗经治的HR+/HER2-晚期乳腺癌患者,对比Dato-DXd与研究者选择的化疗方案(
研究结果显示,Dato-DXd的疗效较化疗组显著更优:Dato-DXd组的中位PFS达6.9个月,显著优于化疗组的4.9个月,疾病进展或死亡风险降低37%(HR=0.63,P<0.0001),为内分泌经治患者带来了长期生存的新希望。亚组分析进一步证实,无论患者既往化疗线数为1线或2线、既往CDK4/6抑制剂治疗持续时间≤12个月或>12个月、既往内分泌治疗时间<6个月或≥6个月、是否存在脑转移,Dato-DXd均较化疗展现出更优的PFS。在肿瘤缓解方面,Dato-DXd的表现同样优异:Dato-DXd组的客观缓解率(ORR)达36.4%,高于化疗组的22.9%,表明Dato-DXd具有良好的抗肿瘤活性,可为该人群带来显著的肿瘤缓解[2]。
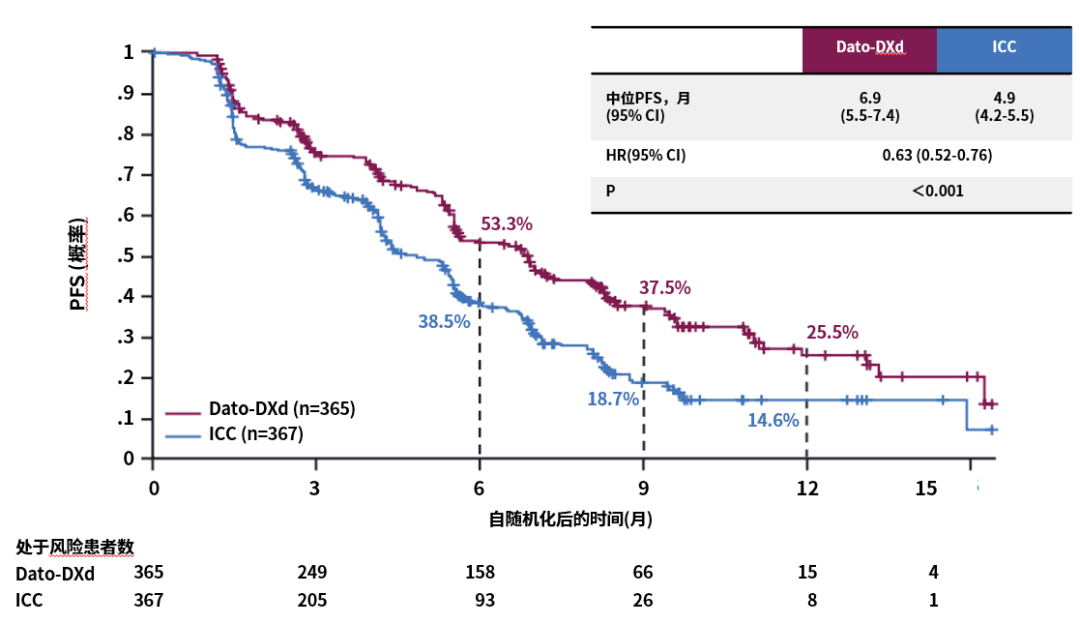
图1 TB01研究PFS分析[2]
值得关注的是,Dato-DXd在中国人群中的表现更为突出,Dato-DXd组的中位PFS达8.1个月,显著高于化疗组的4.2个月,疾病进展或死亡风险降低46%(HR=0.54,P=0.0329)[3]。这提示中国患者可能对Dato-DXd治疗更为敏感,为中国临床诊疗决策提供参考。
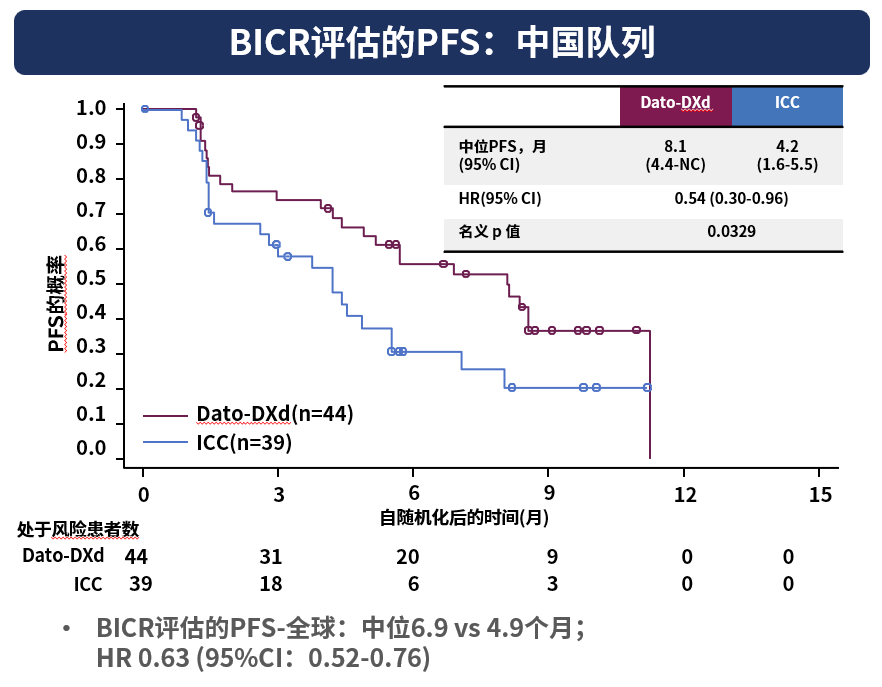
图2 TB01研究中国队列PFS分析[3]
在HER2 IHC 0的患者中,Dato-DXd同样展现出显著治疗优势:Dato-DXd组的中位PFS达到7.1个月,优于化疗组的4.4个月(HR=0.60)[4]。该结果提示,HER2 IHC 0人群可能是Dato-DXd治疗的优选人群,为临床精准筛选患者提供了有力循证依据。
在安全性方面,Dato-DXd组≥3级治疗相关不良事件为化疗组的一半(20.8% vs. 44.7%)且血液学不良反应发生率较低。Dato-DXd相关特殊不良事件多为1-2级,临床可通过对症处理有效管理,整体不良事件可防可控[2]。
基于TB01研究的积极数据,2025年8月,Dato-DXd已获国家药品监督管理局(NMPA)批准上市,用于治疗既往接受过内分泌治疗且在晚期疾病阶段接受过至少一线化疗的不可切除或转移性的HR+/HER2-(IHC 0、IHC 1+或IHC 2+/ISH-)乳腺癌成人患者,并获国内外权威指南一致推荐[5-7],为该人群带来了新的治疗曙光。
小结
从TB01研究的突破性数据到真实临床实践的快速转化,Dato-DXd已为内分泌经治的HR+/HER2-晚期乳腺癌患者带来了切实的生存获益。其在中国人群中的优异表现,更凸显了该药在本土临床实践中的应用价值和广泛前景。Dato-DXd在国内的临床可及,也标志着我国HR+/HER2-晚期乳腺癌精准治疗将迈向新高度。未来,期待Dato-DXd等ADC药物持续向更前线、更广泛的治疗领域探索突破,照亮更多乳腺癌患者的生命之路!
编辑:River
审校:River
排版:Seren
执行:Ocean
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。